题目内容
12.2015年“世界水日”和“中国水周”活动的宣传主题为“节约水资源,保障水安全”. 下列关于水的认识不正确的( )| A. | 水中Ca2+、Mg2+的增多会引起水体富营养化 | |
| B. | 电解水实验可证明水是由氢、氧两种元素组成 | |
| C. | 生活中可以用煮沸的方法能降低水的硬度 | |
| D. | 水经过“三态”变化实现在自然界中的循环 |
分析 A、根据水体的富营养化污染原因考虑;
B、根据电解水实验的结论解答;
C、根据根据硬水软化的特点考虑;
D、根据水在自然界中有固态、液态、气态三态变化解答.
解答 解:
A、水中氮和钾元素的增多会引起水体的富营养化污染,水中Ca2+、Mg2+的增多会使水的硬度增大,故说法错误.
B、电解水生成了氢气和氧气,证明了水是由氢、氧两种元素组成的.故说法正确.
C、硬水软化的方法有:蒸馏和煮沸,故说法正确;
D、水在自然界中有固态、液态、气态三态变化,能以三态形式存在,通过“三态”变化实现在自然界中的循环,故故说法正确;
答案:A
点评 解答本题关键是要知道水是一种最常见的溶剂,知道地球中水和淡水的含量情况,了解硬水软化的方法,知道水体富营养化的原因.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
3.某兴趣小组将一小包铜粉和锌粉的混合物放入一定量的硝酸银溶液中,使其成分反应后过滤,得到滤液A和固体B,并对滤液的组成进行研究.
【提出问题】滤液中的溶质可能有哪些?
【提出猜想】①只有Zn(NO3)2②Zn(NO3)2、AgNO3③Zn(NO3)2、Fe(NO3)2④Zn(NO3)2、AgNO3、Fe(NO3)2
【交流讨论】不合理的猜想是②(填标号),其理由是硝酸银能和铁反应生成硝酸亚铁和银;
【实验探究一】若猜想①成立,通过以下实验课确定固体B的成分,请将下表填写完整.
【实验探究二】若猜想④成立,小组同学欲从该废液中回收银,并得到副产品硫酸亚铁晶体.实验方案如下:
(1)固体甲中含有的物质是(填化学式)Fe、Ag;溶液乙的化学式为Zn(NO3)2、Fe(NO3)2.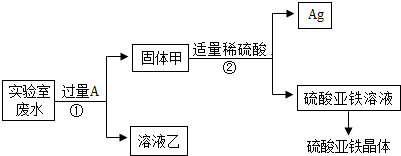
(2)写出步骤①的化学方程式:Fe+2AgNO3=Fe(NO3)2+2Ag.
【实验探究三】银、铁、铜是日常生活中经常接触到的三种金属,对Ag、Fe、Cu三种金属活动顺序的探究,下列所选试剂组不可行的是②.
①Fe、Ag、CuSO4溶液;②Cu、Ag、FeSO4溶液;③Cu、FeSO4溶液、AgNO3溶液
在你认为可行的试剂组中,写出其中发生反应的化学方程式Fe+CuSO4═FeSO4+Cu(若可行的试剂不只一组,请任选其中一组).
【提出问题】滤液中的溶质可能有哪些?
【提出猜想】①只有Zn(NO3)2②Zn(NO3)2、AgNO3③Zn(NO3)2、Fe(NO3)2④Zn(NO3)2、AgNO3、Fe(NO3)2
【交流讨论】不合理的猜想是②(填标号),其理由是硝酸银能和铁反应生成硝酸亚铁和银;
【实验探究一】若猜想①成立,通过以下实验课确定固体B的成分,请将下表填写完整.
| 实验步骤 | 现象 | 有关反应的化学方程式 |
| 要少量固体B,滴加 稀盐酸 | 有气泡产生 | Zn+2HCl═ZnCl2+H2↑ |
(1)固体甲中含有的物质是(填化学式)Fe、Ag;溶液乙的化学式为Zn(NO3)2、Fe(NO3)2.

(2)写出步骤①的化学方程式:Fe+2AgNO3=Fe(NO3)2+2Ag.
【实验探究三】银、铁、铜是日常生活中经常接触到的三种金属,对Ag、Fe、Cu三种金属活动顺序的探究,下列所选试剂组不可行的是②.
①Fe、Ag、CuSO4溶液;②Cu、Ag、FeSO4溶液;③Cu、FeSO4溶液、AgNO3溶液
在你认为可行的试剂组中,写出其中发生反应的化学方程式Fe+CuSO4═FeSO4+Cu(若可行的试剂不只一组,请任选其中一组).
4.某食品包装中防腐剂的主要成分是铁粉和生石灰,某化学兴趣小组对一包久置的这种防腐剂固体样品进行探究.
【提出问题】久置固体的成分是什么?
【查阅资料】常温下,铁与氯化铁溶液发生反应生成氯化亚铁.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3
【实验探究】
方案(一):
方案二:将久置固体研碎并用磁铁充分吸引,取剩余固体用足量蒸馏水溶解过滤
【反思评价】通过以上实验,仍然不能确定是否含有的物质是CaO、Ca(OH)2.
【提出问题】久置固体的成分是什么?
【查阅资料】常温下,铁与氯化铁溶液发生反应生成氯化亚铁.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3
【实验探究】
方案(一):
| 实验操作 | 实验现象 | 实验结论 |
| 取少量久置固体于试管中,加入足量稀盐酸. | 固体逐渐消失,有大量气泡产生,得到浅绿色溶液 | 固体中一定含有Fe,一定不含Fe2O3 |
实验操作 | 实验现象 | 实验结论 |
| 1.取少量滤液于试管中,加入碳酸钠溶液 | 产生白色沉淀 | 反应的化学方程式是 Ca(OH)2+Na2CO3═CaCO3↓+2NaOH |
| 2.取少量滤渣于试管中,加入足量稀盐酸,将生成的气体通入澄清的石灰水 | ①固体逐渐消失,有大量气泡产生,得到黄色溶液 ②澄清的石灰水变浑浊 | 固体中一定含有 Fe2O3和CaCO3 |
11.推理是学习中常用的方法,现有以下推理结果,其中正确的是( )
| A. | 酸溶液的PH<7,则PH<7的溶液一定是酸溶液 | |
| B. | 点燃H2和O2的混合气体可能发生爆炸,则点燃CH4与O2的混合气体也可能发生爆炸 | |
| C. | 化学反应有四种基本类型,则四种基本类型能包括所有的化学反应 | |
| D. | 分子是原子构成的,而原子不一定都能构成分子 |
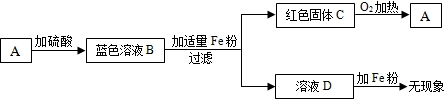
 A-F均为初中化学中常见的物质,其中A、C的组成元素相同,D是红色单质.如图是它们之间的转化关系,请回答下列问题:
A-F均为初中化学中常见的物质,其中A、C的组成元素相同,D是红色单质.如图是它们之间的转化关系,请回答下列问题: ,表示的是一种金属阳离子.
,表示的是一种金属阳离子.
 B.
B. C.
C. D.
D.