题目内容
10.对以下实验的实验现象描述,正确的是( )| A. | 铁在空气中剧烈燃烧,生成黑色固体 | |
| B. | 氯化铵固体和熟石灰混合研磨,生成无色无味的气体 | |
| C. | 分别点燃一小块棉纤维和羊毛纤维,都产生了烧焦羽毛的气味 | |
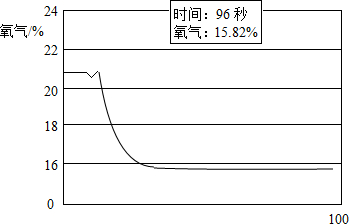
| D. | 把带有火星的木条伸入盛有氧气的集气瓶中,木条复燃 |
分析 A、根据铁在空气中不能燃烧进行分析判断.
B、根据氯化铵固体和熟石灰混合研磨的现象进行分析判断.
C、根据分别点燃一小块棉纤维和羊毛纤维的现象进行分析判断.
D、根据把带有火星的木条伸入盛有氧气的集气瓶中中的现象进行分析判断.
解答 解:A、铁在空气中不能燃烧,故选项说法错误.
B、氯化铵固体和熟石灰混合研磨,生成有刺激性气味的气体,故选项说法错误.
C、点燃一小块棉纤维不产生烧焦羽毛的气味,故选项说法错误.
D、氧气能支持燃烧,把带有火星的木条伸入盛有氧气的集气瓶中,木条复燃,故选项说法正确.
故选:D.
点评 本题难度不大,掌握常见物质燃烧的现象即可正确解答;在描述物质燃烧的现象时,需要注意光和火焰、烟和雾的区别.

练习册系列答案
相关题目
5.家庭厨房常用的下列物质与水混合,不能形成溶液的是( )
| A. | 碱面 | B. | 植物油 | C. | 白糖 | D. | 食盐 |
2.某混合气体可能含有CO,H2,CO2,HCl,N2中的以一种或几种,依次进行以下实验(假设每步反应都完全进行).
①通过一定量澄清石灰水不变浑浊;
②通过CaCl2溶液不变浑浊;
③通过浓硫酸,再通过灼热的CuO时,固体变成红色;
④通过澄清石灰水变浑浊;
⑤通过无水硫酸铜变蓝.
下列对原混合气体的判断正确的是( )
①通过一定量澄清石灰水不变浑浊;
②通过CaCl2溶液不变浑浊;
③通过浓硫酸,再通过灼热的CuO时,固体变成红色;
④通过澄清石灰水变浑浊;
⑤通过无水硫酸铜变蓝.
下列对原混合气体的判断正确的是( )
| A. | 可能同时含有CO2和HCl,一定含有一氧化碳,可能含有氢气 | |
| B. | 一定无CO2,一定有CO,可能有H2 | |
| C. | 同时含有CO2和CO,不一定有H2 | |
| D. | 一定无CO2,一定有CO和H2 |
19. 20℃时,在两只各盛有50克水的烧杯中,分别加入30克氯化钠和蔗糖固体,搅拌使其充分溶解,结果如图所示.下列说法正确的是( )
20℃时,在两只各盛有50克水的烧杯中,分别加入30克氯化钠和蔗糖固体,搅拌使其充分溶解,结果如图所示.下列说法正确的是( )
 20℃时,在两只各盛有50克水的烧杯中,分别加入30克氯化钠和蔗糖固体,搅拌使其充分溶解,结果如图所示.下列说法正确的是( )
20℃时,在两只各盛有50克水的烧杯中,分别加入30克氯化钠和蔗糖固体,搅拌使其充分溶解,结果如图所示.下列说法正确的是( )| A. | 两烧杯中的溶液质量相等 | B. | 20℃时两者的溶解度相等 | ||
| C. | 氯化钠溶液一定是饱和溶液 | D. | 蔗糖溶液一定是饱和溶液 |
20.(1)实验室给你提供了下列仪器,请选用合适的仪器完成指定的实验.

①图中仪器d的名称是:长颈漏斗.
②要制取较多的O2用来探究其性质(要求制取过程中可以添加反应物),组装气体发生装置需要的仪器是adf(填序号,下同),请写出该反应的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,收集氧气应采用向上排空气法法,这种收集方法是根据氧气的密度比空气的密度大性质.
③提纯粗盐时,过滤需要选用上述仪器中的eh(填序号),除此之外还缺少的仪器是滤纸、漏斗、玻璃棒(填名称).
(2)为探究气体X的组成,某兴趣小组进行如图所示实验(固定装置未画出).
【资料在线】
①加热条件下,气体X能与氧化铜反应生成铜、水和氮气.
②碱石灰为固体氢氧化钠和氢氧化钙的混合物,不与气体X反应.无水氯化钙可吸收气体X.
③本实验条件下,氮气密度为1.15g•L-1,装置内空气中的水与二氧化碳对相关数据测定的影响可忽略不计.【实验步骤】
①连接仪器,并检查装置气密性.
②取一定量氧化铜,准确称得其质量为2.40g.
③按图所示装入药品(其中B、C管中分别装入的是足量碱石灰和足量无水氯化钙),测并记录相在数据Ⅰ(见表).
④连接A、B、C装置,将气体X缓缓通入一段时间后,连接上D装置,读数后开始加热.当A装置中氧化铜反应完全,停止加热,继续通入气体X至玻璃管冷却后,再次测量并记录相关数据Ⅱ(见表).
【实验装置】

【相关数据】
【回答问题】
①B中装置中氧化钙吸水的原理为CaO+H2O=Ca(OH)2(用化学方程式表示).
②实验过程中,当观察到D装置中量气管的液面不再下降,说明氧化铜已反应完全,停止加热,继续通入气体X至玻璃管冷却的目的是防止空气进入把生成的铜氧化,造成误差.
③分析实验测量的数据,生成水的质量为0.54g,氧化铜中氧元素的质量为0.48g.由此推知,气体X中一定没有(填“有”或“没有”)氧元素.
④通过计算推导出气体X的化学式为NH3;气体X还原氧化铜的化学方程式为:2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+3H2O+N2.

①图中仪器d的名称是:长颈漏斗.
②要制取较多的O2用来探究其性质(要求制取过程中可以添加反应物),组装气体发生装置需要的仪器是adf(填序号,下同),请写出该反应的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,收集氧气应采用向上排空气法法,这种收集方法是根据氧气的密度比空气的密度大性质.
③提纯粗盐时,过滤需要选用上述仪器中的eh(填序号),除此之外还缺少的仪器是滤纸、漏斗、玻璃棒(填名称).
(2)为探究气体X的组成,某兴趣小组进行如图所示实验(固定装置未画出).
【资料在线】
①加热条件下,气体X能与氧化铜反应生成铜、水和氮气.
②碱石灰为固体氢氧化钠和氢氧化钙的混合物,不与气体X反应.无水氯化钙可吸收气体X.
③本实验条件下,氮气密度为1.15g•L-1,装置内空气中的水与二氧化碳对相关数据测定的影响可忽略不计.【实验步骤】
①连接仪器,并检查装置气密性.
②取一定量氧化铜,准确称得其质量为2.40g.
③按图所示装入药品(其中B、C管中分别装入的是足量碱石灰和足量无水氯化钙),测并记录相在数据Ⅰ(见表).
④连接A、B、C装置,将气体X缓缓通入一段时间后,连接上D装置,读数后开始加热.当A装置中氧化铜反应完全,停止加热,继续通入气体X至玻璃管冷却后,再次测量并记录相关数据Ⅱ(见表).
【实验装置】

【相关数据】
| 测量项目/数据编号 | Ⅰ | Ⅱ |
| 玻璃管(含药品)的质量/g | 52.40 | 51.92 |
| B装置(含药品)的质量/g | 102.00 | 102.54 |
| 氮气的体积/mL | / | 243.5 |
①B中装置中氧化钙吸水的原理为CaO+H2O=Ca(OH)2(用化学方程式表示).
②实验过程中,当观察到D装置中量气管的液面不再下降,说明氧化铜已反应完全,停止加热,继续通入气体X至玻璃管冷却的目的是防止空气进入把生成的铜氧化,造成误差.
③分析实验测量的数据,生成水的质量为0.54g,氧化铜中氧元素的质量为0.48g.由此推知,气体X中一定没有(填“有”或“没有”)氧元素.
④通过计算推导出气体X的化学式为NH3;气体X还原氧化铜的化学方程式为:2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+3H2O+N2.