题目内容
9.现有氯酸钾和二氧化锰的混合物共4g,加热使其充分反应,冷却,称得残余固体的质量为3.04g.求:生成氧气的质量为多少?原固体混合物中二氧化锰的质量为多少?分析 反应前后的质量差即为反应生成氧气的质量;
根据氧气的质量可以计算氯酸钾的质量,二氧化锰的质量即可解答.
解答 解:反应生成氧气的质量为:4g-3.04g=0.96g,
设氯酸钾的质量为x,
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,
245 96
x 0.96g
$\frac{245}{x}=\frac{96}{0.96g}$
x=2.45g
二氧化锰占混合物的质量=4g-2.45g=1.55g
答案:生成氧气的质量为2.45g;原固体混合物中二氧化锰的质量为1.55g.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
11.如图所示实验操作不正确的是( )
| A. |  读取液体体积 | B. |  过滤 | C. |  倾倒液体 | D. |  制取二氧化碳 |
14.下列关于同种元素组成的物质说法错误的是( )
| A. | 可以是单质 | B. | 可以是混合物 | C. | 可以是纯净物 | D. | 可以是化合物 |
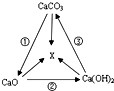 氢氧化钠与氢氧化钙是初中化学最常见的两种碱,根据你所学知识回答:
氢氧化钠与氢氧化钙是初中化学最常见的两种碱,根据你所学知识回答: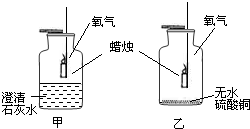 某同学为了研究蜡烛燃烧的产物,设计了以下实验,如图所示.在甲、乙两集气瓶中充满氧气,瓶底分别装有澄清的石灰水和无水硫酸铜白色固体.
某同学为了研究蜡烛燃烧的产物,设计了以下实验,如图所示.在甲、乙两集气瓶中充满氧气,瓶底分别装有澄清的石灰水和无水硫酸铜白色固体.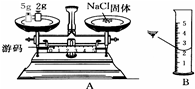 实验室欲配制30g质量分数为25%的NaCl溶液,有下列操作:a.用量筒量取水,b.用天平称取所需氯化钠,c.所需食盐与水混合后搅拌溶解,d.计算所需食盐和水的质量,e.溶液的转存并贴标签.试回答下列问题.
实验室欲配制30g质量分数为25%的NaCl溶液,有下列操作:a.用量筒量取水,b.用天平称取所需氯化钠,c.所需食盐与水混合后搅拌溶解,d.计算所需食盐和水的质量,e.溶液的转存并贴标签.试回答下列问题.