题目内容
只用一种试剂就能够将NaOH、NaCl、HCl三种溶液分开,该试剂是( )
| A、AgN03溶液 |
| B、BaCl2溶液 |
| C、紫色石蕊试液 |
| D、无色酚酞试液 |
考点:酸、碱、盐的鉴别
专题:物质的鉴别题
分析:能将NaOH、NaCl、HCl三种溶液鉴别出来的一种试剂应能与三种待鉴别溶液混合时出现明显不同的三种现象,利用复分解反应规律分析选项中的物质与待鉴别物质所发生反应的情况,做出判断.
解答:解;A、硝酸银遇三种溶液都会产生沉淀,现象相同.所以使用硝酸银溶液不能将NaOH、NaCl、HCl三种溶液鉴别出来,故A错误;
B、氯化钡和三种溶液都不反应,混合都无现象.所以氯化钡溶液不能把NaOH、NaCl、HCl这三种溶液区分开.故B错误;
C紫色石蕊溶液遇NaOH溶液能变蓝色、遇NaCl溶液不变色,遇HCl溶液变红色.所以紫色石蕊溶液能将NaOH、NaCl、HCl三种溶液鉴别出来,故C正确;
D、虽然酚酞试液遇NaOH溶液能变红色,但与NaCl、HCl溶液混合时无明显现象.所以使用酚酞试液不能将NaOH、NaCl、HCl三种溶液鉴别出来,故D错误;
故选项为:C.
B、氯化钡和三种溶液都不反应,混合都无现象.所以氯化钡溶液不能把NaOH、NaCl、HCl这三种溶液区分开.故B错误;
C紫色石蕊溶液遇NaOH溶液能变蓝色、遇NaCl溶液不变色,遇HCl溶液变红色.所以紫色石蕊溶液能将NaOH、NaCl、HCl三种溶液鉴别出来,故C正确;
D、虽然酚酞试液遇NaOH溶液能变红色,但与NaCl、HCl溶液混合时无明显现象.所以使用酚酞试液不能将NaOH、NaCl、HCl三种溶液鉴别出来,故D错误;
故选项为:C.
点评:本题考查物质的检验和鉴别,应用物质的化学性质来鉴别物质时,必须明确发生化学反应时的现象,题目难度不大.

练习册系列答案
相关题目
食醋中通常含有3%-5%的醋酸,则下列关于食醋的用途不正确的是( )
| A、吃松花蛋时蘸醋可消除涩味 |
| B、可用于清除去水垢 |
| C、儿童误食生石灰时可喝醋缓解 |
| D、治疗胃酸过多 |
下列实验操作中,不正确的是( )
A、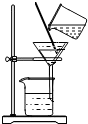 过滤 |
B、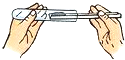 取固体粉末 取固体粉末 |
C、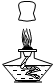 熄灭酒精灯 |
D、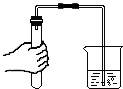 检查气密性 检查气密性 |
由
、
、
、
,按不同的组合,可形成化合物最多有( )
| +1 |
| H |
| -2 |
| O |
| +6 |
| S |
| +1 |
| K |
| A、5种 | B、6种 | C、7种 | D、8种 |
等质量的SO2和SO3中氧元素的质量比为( )
| A、4:5 | B、3:2 |
| C、5:6 | D、2:3 |
小明午餐时喝汤,感觉汤太咸,于是便向汤中倒了一些开水后,感觉可口多了.如果将汤理解为氯化钠溶液,那么小明“感觉可口多了”是因为( )
| A、溶液中溶质的质量分数减小了 |
| B、溶液的质量增加了 |
| C、溶液中溶质的质量减少了 |
| D、溶质的溶解度减小了 |
下列物质中,属于纯净物的是( )
| A、蒸馏水 | B、雪碧饮料 |
| C、海水 | D、清新空气 |