题目内容
7. 铁是生活中的常见金属,请回答下列问题:
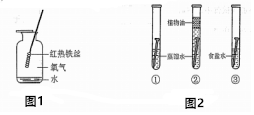
铁是生活中的常见金属,请回答下列问题:(1)如图1是细铁丝在氧气中然撒后的装置图,集气瓶中水的作用是防止生成物熔化溅落下来炸裂集气瓶.
(2)某学习小组用相同的光亮铁钉探究生锈与哪些因素有关,设计的实验如图2中①-③所示,对比试管①②,得出铁生锈需要与氧气接触,实验②与实验①(填序号)进行对比,涉及实验③的目的是食盐能否加快铁的锈蚀速率.
分析 (1)根据铁丝在氧气中燃烧的注意事项来分析;
(2)根据铁生锈的条件是跟空气和水同时接触分析.
解答 解:(1)铁丝在氧气中燃烧实验,集气瓶底部要预先放少量的水或铺一层细沙,目的是防止生成物熔化溅落下来炸裂集气瓶;故填:防止生成物熔化溅落下来炸裂集气瓶;
(2)①中的铁钉既与水接触,又与氧气接触,所以铁钉发生了锈蚀,而②中的铁钉只与水接触没有锈蚀,说明铁钉锈蚀需要氧气;实验③中的铁钉锈蚀速率比①中的快,这说明该实验在探究食盐能否加快铁的锈蚀速率;故填:氧气;①;食盐能否加快铁的锈蚀速率.
点评 本题主要考查学生对铁生锈的条件这一知识点的掌握情况,尤其强调铁同时直接和氧气、水接触这一点.

练习册系列答案
相关题目
15.下列化学方程式书写正确的是( )
| A. | 2KClO3$\frac{\underline{\;△\;}}{\;}$2KCl+3O2↑ | B. | 4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | ||
| C. | 2Ag+Cu(NO3)2═2AgNO3+Cu↓ | D. | 2HCl+Na2SO4═2NaCl+H2SO4 |
12.下列物质中有一种与其他三种物质都能发生反应,它是( )
| A. | 镁 | B. | 稀硫酸 | C. | 碳酸氢钠 | D. | 氢氧化钠 |
2. 下表提供了硝酸钾固体在不同温度时的溶解度.
下表提供了硝酸钾固体在不同温度时的溶解度.
(1)由上表可以总结出硝酸钾的溶解度随温度变化的趋势是硝酸钾中的溶解度随温度的升高而增加.
(2)20℃时,向50g水中加入15.8g硝酸钾,充分溶解后得到饱和(选填:饱和或不饱和)溶液,溶液的溶质质量分数为24.0%.
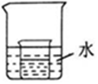
(3)如图所示,小烧杯中盛放的是上述(2)中所得的硝酸钾溶液,若将少量的下列固态物质分别小心地加入到大烧杯的水中,不断搅拌,则小烧杯中一定有硝酸钾晶体析出的是ac(填字母).
a.冰 b.生石灰 c.硝酸铵 d.氢氧化钠
(4)40℃时,向100g水中加入80g硝酸钾若要使硝酸钾完全溶解,可以采用的措施有加入水或升温.
(5)现有60℃的硝酸钾饱和溶液210g,若降温至20℃,析出硝酸钾晶体的质量是78.4g;通过过滤操作可将析出的硝酸钾晶体和溶液分离.
(6)现有80℃时溶质质量分数为30%的硝酸钾溶液,则至少降温到b(温度范围)才能得到硝酸钾针状晶体.
a.0℃-20℃b.20℃-40℃c.40℃-60℃d.60℃-80℃
 下表提供了硝酸钾固体在不同温度时的溶解度.
下表提供了硝酸钾固体在不同温度时的溶解度.| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| 溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 |
(2)20℃时,向50g水中加入15.8g硝酸钾,充分溶解后得到饱和(选填:饱和或不饱和)溶液,溶液的溶质质量分数为24.0%.
(3)如图所示,小烧杯中盛放的是上述(2)中所得的硝酸钾溶液,若将少量的下列固态物质分别小心地加入到大烧杯的水中,不断搅拌,则小烧杯中一定有硝酸钾晶体析出的是ac(填字母).
a.冰 b.生石灰 c.硝酸铵 d.氢氧化钠
(4)40℃时,向100g水中加入80g硝酸钾若要使硝酸钾完全溶解,可以采用的措施有加入水或升温.
(5)现有60℃的硝酸钾饱和溶液210g,若降温至20℃,析出硝酸钾晶体的质量是78.4g;通过过滤操作可将析出的硝酸钾晶体和溶液分离.
(6)现有80℃时溶质质量分数为30%的硝酸钾溶液,则至少降温到b(温度范围)才能得到硝酸钾针状晶体.
a.0℃-20℃b.20℃-40℃c.40℃-60℃d.60℃-80℃
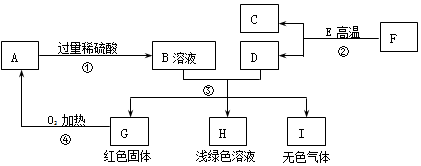
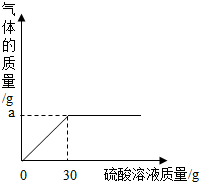 草木灰属于农家肥料,它的主要成分是碳酸钾,还有硫酸钾,氯化钾等,为测定某草木灰样品中的有效成分,取100g该草木灰于烧杯中,不断滴入稀硫酸溶液,当滴入30g稀硫酸时,不再有气泡产生,此时烧杯中的残余混合物质量为127.8g,碳酸钾与硫酸反应的化学方程式为K2CO3+H2SO4=K2CO4+CO2↑+H2O
草木灰属于农家肥料,它的主要成分是碳酸钾,还有硫酸钾,氯化钾等,为测定某草木灰样品中的有效成分,取100g该草木灰于烧杯中,不断滴入稀硫酸溶液,当滴入30g稀硫酸时,不再有气泡产生,此时烧杯中的残余混合物质量为127.8g,碳酸钾与硫酸反应的化学方程式为K2CO3+H2SO4=K2CO4+CO2↑+H2O 我们已经知道空气的主要成分是氮气和氧气,如图所示为测定空气中氧气含量的实验装置示意图,图中玻璃管里的活塞可以左右移动,活塞的左端管内有密封的空气,活塞右端的玻璃管口跟空气相通,实验开始前活塞处在刻度5处.请回答下列问题:
我们已经知道空气的主要成分是氮气和氧气,如图所示为测定空气中氧气含量的实验装置示意图,图中玻璃管里的活塞可以左右移动,活塞的左端管内有密封的空气,活塞右端的玻璃管口跟空气相通,实验开始前活塞处在刻度5处.请回答下列问题: