题目内容
18.反应②是工业炼铁的主要原理,F为赤铁矿石的主要成分,A、C、E都是氧化物,D、G、I属于单质,如图是它们之间的相互转化关系.请回答: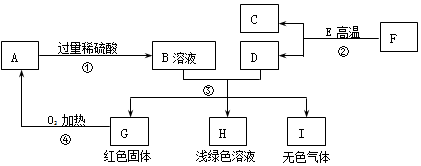
(1)B溶液中所含有的溶质为CuSO4、H2SO4,H溶液显浅绿色,其中所含有的溶质是FeSO4.
(2)写出反应②的化学方程式3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(3)指出物质A和I在加热条件下发生的化学反应的基本反应类型置换反应.
分析 找出突破口,反应②是炼铁工业中的主要反应,F为赤铁矿石的主要成分,即一氧化碳还原氧化铁生成铁和二氧化化碳,再根据A、C、E都是氧化物,D、G、I属于单质,所以E是一氧化碳,C是二氧化碳,D是单质铁,再根据常见现象判断:红色固体是铜、浅绿色溶液是亚铁离子溶液.进一步进行推断.
解答 解:(1)反应②是炼铁工业中的主要反应,F为赤铁矿石的主要成分,即一氧化碳还原氧化铁生成铁和二氧化化碳,再根据A、C、E都是氧化物,D、G、I属于单质,所以E是一氧化碳,C是二氧化碳,D是单质铁,再根据常见现象判断:红色固体G是铜、浅绿色溶液是亚铁离子溶液.由于A是氧化物,而且能和稀硫酸反应,故A是氧化铜,B溶液中含有硫酸铜,由于稀硫酸是过量的,故B溶液中还含有硫酸;由于H是浅绿色溶液,说明其中含有Fe2+.
故答案为:CuSO4、H2SO4;FeSO4;
(2)由于②是炼铁工业中的主要反应,故答案为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(3)I是氢气,A是氧化铜,所以两者加热时发生的反应方程式为:H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O,该反应的反应物生成物均是一种单质和一种化合物,所以属于置换反应.
故答案为:(1)CuSO4、H2SO4; FeSO4;
(2)3CO+Fe2O3 $\frac{\underline{\;高温\;}}{\;}$ 2Fe+3CO2;
(3)置换反应.
点评 本题为框图型物质推断题,完成此类题目,可以依据题干提供的信息,结合框图,找准解题的突破口,直接得出物质的化学式,然后顺推或逆推或由两边向中间推得出其他物质的化学式.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
9.下列关于粒子结构示意图的说法正确的是( )

| A. | ①③可以形成化合物 | |
| B. | ①②③在元素周期表中同一横行 | |
| C. | ②③④都是具有稳定结构的粒子,化学性质相同 | |
| D. | ①②③④表示四种不同的粒子 |
6.向一定量AgNO3、Cu(NO3)2、Zn(NO3)2的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤渣中加入稀硫酸,无气泡产生,则滤渣中一定含有的金属是( )
| A. | 银、铜、铁、锌 | B. | 银 | C. | 银、铜 | D. | 银、铜、铁 |

 A、B、C、D分别是初中化学常见物质金属、酸、碱、盐中的一种.如图A、B、C、D之间的连线表示它们彼此之间能够发生化学反应,其中A与B能发生中和反应,D是目前世界上产量最多的金属.请回答:
A、B、C、D分别是初中化学常见物质金属、酸、碱、盐中的一种.如图A、B、C、D之间的连线表示它们彼此之间能够发生化学反应,其中A与B能发生中和反应,D是目前世界上产量最多的金属.请回答: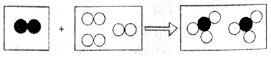 如图是某化学反应的微观模型,“○”“●”分别表示不同元素的原子,下列各项中对图示模型理解正确的是( )
如图是某化学反应的微观模型,“○”“●”分别表示不同元素的原子,下列各项中对图示模型理解正确的是( )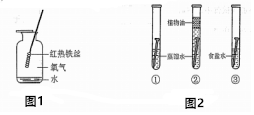 铁是生活中的常见金属,请回答下列问题:
铁是生活中的常见金属,请回答下列问题: