题目内容
8.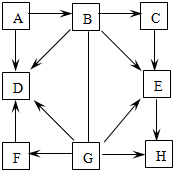 如图中的A~H表示几种初中化学常见的含有氧元素的化合物,其中A、B、D均含钠元素,B、C、E均含碳元素,D、F、G均含硫元素,E、H属于氧化物;B俗称苏打,F与石灰乳可制农药波尔多液.图中“-”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去.
如图中的A~H表示几种初中化学常见的含有氧元素的化合物,其中A、B、D均含钠元素,B、C、E均含碳元素,D、F、G均含硫元素,E、H属于氧化物;B俗称苏打,F与石灰乳可制农药波尔多液.图中“-”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去.(1)F是由离子(选填“分子”、“原子”或“离子”)构成的.
(2)写出有关物质的化学式是D:Na2SO4,H:H2O.
(3)写出A→B反应的化学方程式CO2+2NaOH=Na2CO3+H2O.
(4)写出F→D反应的化学方程式CuSO4+2NaOH=Cu(OH)2↓+Na2SO4.
分析 根据A~H表示几种初中化学常见的含有氧元素的化合物,B俗称苏打,所以B是碳酸钠,F与石灰乳可制农药波尔多液,所以F是硫酸铜,A、B、D均含钠元素,B、C、E均含碳元素,D、F、G均含硫元素,E、H属于氧化物,A会转化成B、D,B会转化成D,所以A是氢氧化钠,D是硫酸钠,G会转化成硫酸铜、硫酸钠,所以G是硫酸,E是含碳氧化物,所以E是二氧化碳,C是碳酸钙,H是水,然后将推出的物质进行验证即可.
解答 解:(1)A~H表示几种初中化学常见的含有氧元素的化合物,B俗称苏打,所以B是碳酸钠,F与石灰乳可制农药波尔多液,所以F是硫酸铜,A、B、D均含钠元素,B、C、E均含碳元素,D、F、G均含硫元素,E、H属于氧化物,A会转化成B、D,B会转化成D,所以A是氢氧化钠,D是硫酸钠,G会转化成硫酸铜、硫酸钠,所以G是硫酸,E是含碳氧化物,所以E是二氧化碳,C是碳酸钙,H是水,经过验证,推导正确,所以F是由离子构成的;
(2)通过推导可知,D是硫酸钠,H是水;故填:Na2SO4;H2O;
(3)A→B反应二氧化碳和氢氧化钠反应产生碳酸钠和水,化学方程式为:;
C→E的反应是碳酸钙在高温的条件下生成氧化钙和二氧化碳,化学方程式为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;
(4)F→D的反应是氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,化学方程式为:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4.
故答案为:(1)离子;
(2)水;
(3)CO2+2NaOH=Na2CO3+H2O;
(4)CuSO4+2NaOH=Cu(OH)2↓+Na2SO4.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

(1)提出问题:这瓶氢氧化钙是否已经生成碳酸钙而变质?
(2)进行猜想:
A、氢氧化钙全部变为碳酸钙;B、氢氧化钙部分变为碳酸钙;C、氢氧化钙没有变质.
(3)设计实验方案进行实验:下表是对猜想A进行实验探究的过程示例:
| 实验步骤 | 实验现象 | 实验结论 |
| 取样,加适量水,搅拌,过滤 ①取少量滤液于试管中,滴入酚酞试液 ②取少量滤渣于试管中,加入盐酸 | ①滤液不变色 ②有气泡产生 | 氢氧化钙全部变为碳酸钙 |
| 实验步骤 | 实验现象 | 实验结论 |
| 取样,加适量水,搅拌,过滤 ①取少量滤液于试管中,滴入酚酞试液 ②取少量滤渣于试管中,加入盐酸 | ①酚酞试液变红色 ②产生气泡 |
①氢氧化钙俗称熟石灰或消石灰农业上一般采用氢氧化钙改良酸性土壤
②氢氧化钙变质是由于与空气中的二氧化碳 发生反应的缘故,反应的化学方程式是Ca(OH)2+CO2═CaCO3↓+H2O,因此氢氧化钠钙应密封 保存.
| A. | 降低饱和溶液的温度,一定有晶体析出 | |
| B. | 长期放置后不会分层的液体不一定是溶液 | |
| C. | 硝酸钾饱和溶液一定比其不饱和溶液质量分数大 | |
| D. | 配制好6%的NaCl溶液,装瓶时不小心撒漏一部分,瓶中NaCl溶液浓度小于6% |

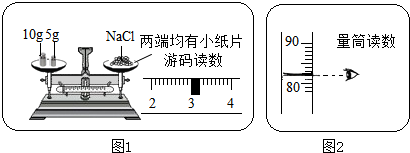
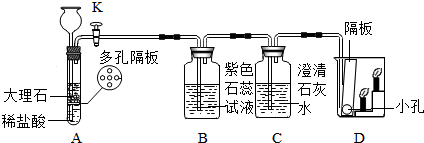
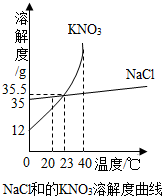 用科学方法认识和改造物质
用科学方法认识和改造物质