题目内容
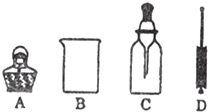
17.如图是配制50g质量分数为5%的氯化钠溶液的相关操作过程示意图:
试回答:
(1)配制该氯化钠溶液的正确的操作顺序是A
A.④⑤①②③B.①②③④⑤C.③④①②⑤D.②①④③⑤
(2)⑤操作中应称量氯化钠的质量是2.5g.放好砝码和游码后,向托盘上加氯化钠时,若指针偏向分度盘的左边,应进行的操作是减少NaCl.
(3)②操作应选用100mL(10 mL、100 mL中选择);量水时,量筒必须平放,视线要跟量筒凹液面的最低处保持水平.
(4)③操作的作用是搅拌,加快氯化钠的溶解速率.
分析 (1)根据配制溶质质量分数一定的溶液的基本步骤,进行分析解答.
(2)利用溶质质量=溶液质量×溶质的质量分数,进行分析解答.
使用托盘天平称量药品时应遵循“左物右码”,称量指定质量的药品,此时先调好砝码和游码,再向左盘增减药品至天平平衡;指针偏向分度盘的左边,说明药品质量大于砝码质量,据此进行分析解答.
(3)从减小实验误差的角度去选择量筒的量程,进行分析解答.
(4)根据③操作是溶解操作,进行分析解答.
解答 解:(1)配制50g质量分数为5%的氯化钠溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解,故正确的操作顺序是④⑤①②③.
(2)溶质质量=溶液质量×溶质的质量分数,配制50g质量分数为5%的氯化钠溶液,需氯化钠的质量=50g×5%=2.5g.
使用托盘天平称量药品时应遵循“左物右码”,称量指定质量的药品,此时先调好砝码和游码,再向左盘增减药品至天平平衡;指针偏向分度盘的左边,说明药品质量大于砝码质量,应减少NaCl.
(3)溶剂质量=溶液质量-溶质质量,则所需水的质量=50g-2.5g=47.5g(合47.5mL),选取量筒时,尽量选用能一次量取的最小规格的量筒.量取47.5mL水时,应选择100mL的量筒.量水时,量筒必须平放,视线要跟量筒凹液面的最低处保持水平.
(4)③操作是溶解操作,作用是搅拌,加快氯化钠的溶解速率.
故答案为:(1)A;(2)2.5g;减少NaCl;(3)100mL;最低;(4)搅拌,加快氯化钠的溶解速率.
点评 本题难度不大,明确配制一定溶质质量分数的溶液实验步骤、注意事项等是正确解答本题的关键.

练习册系列答案
相关题目
5.下列各组溶液,不用其他试剂无法鉴别的是( )
| A. | H2SO4 NaCl Na2CO3 CaCl2 | B. | HCl NaOH CuSO4Mg SO4 | ||
| C. | Na2CO3 K2SO4 BaCl2 HCl | D. | NaNO3 HCl CaCl2 KOH |
12.食品包装袋中常用脱氧剂.某化学兴趣小组将脱氧剂封口打开,将其倒在滤纸上,观察到脱氧剂大部分为黑色粉末,其中还夹杂着少量红色粉末.
【提出问题】该脱氧剂的黑色、红色粉末各是什么?
【提出猜想】黑色粉末可能含碳粉、铁粉、氧化铜中的一种或几种,红色粉末可能含有氧化铁、铜粉中的一种或几种.
【进行实验】
【得出结论】
由实验①②可知,脱氧剂中黑色粉末肯定含铁粉、碳粉,脱氧剂中的红色粉末肯定不含铜,肯定含氧化铁,写出肯定含红色粉末的理由是(用化学方程式表示)Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.

【拓展延伸】小明认为铁生锈时会消耗氧气,因此可用此脱氧剂(实验室可滴几滴水)测定空气中氧气的含量,装置如图所示,集气瓶的实际容积是150ml,量筒内盛100ml的水,当量筒内水面不再变化,且温度恢复至室温时,读出水面在73ml刻度处,由上述实验数据可以算出空气中氧气的体积分数是18%,本实验的测量结果与理论值不一致,原因可能是脱氧剂不足等.
【提出问题】该脱氧剂的黑色、红色粉末各是什么?
【提出猜想】黑色粉末可能含碳粉、铁粉、氧化铜中的一种或几种,红色粉末可能含有氧化铁、铜粉中的一种或几种.
【进行实验】
| 实验编号 | 实验操作 | 实验现象 |
| ① | 取脱氧剂粉末加入足量稀硫酸 | 粉末几乎全被溶解,只有少量黑色粉末为溶解,有气泡产生,溶液变成黄色 |
| ② | 取实验①的残渣灼烧,内壁涂有澄清石灰水的小烧杯罩在上方 | 澄清石灰水变浑浊 |
由实验①②可知,脱氧剂中黑色粉末肯定含铁粉、碳粉,脱氧剂中的红色粉末肯定不含铜,肯定含氧化铁,写出肯定含红色粉末的理由是(用化学方程式表示)Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.

【拓展延伸】小明认为铁生锈时会消耗氧气,因此可用此脱氧剂(实验室可滴几滴水)测定空气中氧气的含量,装置如图所示,集气瓶的实际容积是150ml,量筒内盛100ml的水,当量筒内水面不再变化,且温度恢复至室温时,读出水面在73ml刻度处,由上述实验数据可以算出空气中氧气的体积分数是18%,本实验的测量结果与理论值不一致,原因可能是脱氧剂不足等.
2.生活中的下列变化中,属于化学变化的是( )
| A. | 食物消化 | B. | 木柴折断 | C. | 水分蒸发 | D. | 石蜡熔化 |
9.下列说法中,与化学变化中遵循的质量守恒定律不相符的是( )
| A. | 水变成水蒸气后体积变大,但是质量保持不变 | |
| B. | 镁条在空气中燃烧后,固体质量增加 | |
| C. | 蜡烛燃烧后,质量减少 | |
| D. | 12g碳在40g氧气中充分燃烧,只生成44g二氧化碳 |
7.中考前,我省对初中毕业生进行了化学实验操作考查,老师为同学们提供了几种无标签的固体和液体,要求对固体和液体的反应进行探究.
(1)请你帮助他完成下列探究报告.
(2)现提供以下实验装置,要制取猜想的气体,依据的化学反应的原理是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑(用化学方程式表示).你选择的发生装置和收集装置分别是B 和C或D(填装置序号).
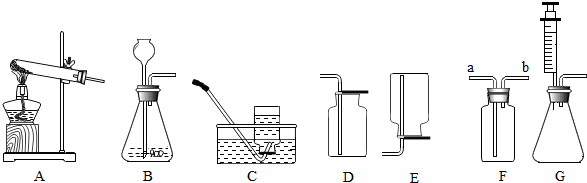
(3)如果用图F装置收集该气体,该气体应由a(填“a”或“b”,下同)端进入.若取用该储气瓶中的气体,应从a端向储气瓶中注水.
(1)请你帮助他完成下列探究报告.
| 猜想与假设 | 操作方法 | 证明猜想正确的实验现象 |

(3)如果用图F装置收集该气体,该气体应由a(填“a”或“b”,下同)端进入.若取用该储气瓶中的气体,应从a端向储气瓶中注水.