题目内容
13.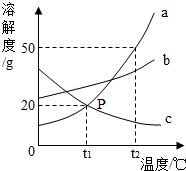 如图是a、b、c三种固体物质的溶解度曲线.
如图是a、b、c三种固体物质的溶解度曲线.(1)曲线上P点表示t1℃是a c的溶解度相等为20g
(2)t2℃时a、b、c三种物质的溶解度由大到小的顺序是a>b>c(填写符合,下同);
(3)要使接近饱和的c物质的溶液变为饱和溶液,可采取的措施有升高温度、蒸发溶剂、增加溶质.
(4)若要从a中含有少量b的混合溶液中提纯b,可用的方法降温结晶.
(5)现有等质量t2℃时的a、b、c三种物质的饱和溶液,将其都降温至t1℃时,析出溶质最多的是a,溶质质量分数最小的是c;
(6)t2℃时,30ga物质加入到50g水中不断搅拌,不能(填写“能”或“不能”)形成80g的溶液.
分析 由溶解度曲线,可以比较t2℃时的a、b、c三种物质的溶解度大小;由c的溶解度受温度的变化影响趋势,可以确定接近饱和的c物质的溶液变为饱和溶液的方法;判断通过降温还是蒸发溶剂的方法达到提纯物质的目的;由t2℃时,a的溶解度,可以计算50g水中最多能溶解 a物质的质量
解答 解:(1)P点是曲线ac的交点,故其含义为t1℃是a c的溶解度相等为20g;
(2)由t2℃时三曲线的位置关系可知,t2℃时a、b、c三种物质的溶解度由大到小的顺序a>b>c;
(3)c的溶解度随着温度的升高而减小,故使接近饱和的c物质的溶液变为饱和溶液,可采取升高温度或蒸发溶剂、增加溶质等方法;
(4)由于a和b的溶解度都随温度的升高而增大,但a的溶解度受温度的影响大,b的溶解度受温度的影响很小,因此若要从a中含有少量b的混合溶液中提纯a,应采取降温结晶的方法,故答案为:降温结晶;
(5)由溶解度曲线图,对比abc三物质溶解度受温度影响大小,可以知道t2℃时三种物质的溶解度a>b>c,从t2℃降温到t1℃,A的溶解度变化较大,所以A析出的较多;c的溶解度随温度的升高而减小,从t2℃降温到t1℃,c无晶体析出.
(6)t2℃时,a的溶解度为50g,故50g水中最多能溶解 a物质25g,形成75g溶液.
故答案为:(1)t1℃是a c的溶解度相等为20g;
(2)a>b>c;
(3)升高温度或蒸发溶剂、增加溶质;
(4)降温结晶;
(5)a、c;
(6)不能.
点评 主要考查了对固体溶解度的概念的理解和固体溶解度曲线的意义,以此培养学生的理解能力、培养学生分析问题、解决问题的能力

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.把17.1g氯化钠和碳酸钠的混合物,加入100g7.3%的盐酸中,恰好完全反应.计算:
(1)生成气体的质量和体积(标准状况下二氧化碳的密度为1.96g/L).
(2)反应后所得溶液中溶质的质量分数.
(1)生成气体的质量和体积(标准状况下二氧化碳的密度为1.96g/L).
(2)反应后所得溶液中溶质的质量分数.
1.一块4克的合金,与足量的盐酸反应,产生0.2克氢气,则该合金的组成可能为( )
| A. | Fe Mg | B. | Fe Al | C. | Fe Zn | D. | Al Mg |
18.下列物质能通过金属与酸反应制得的是 ( )
| A. | CuCl2 | B. | MgSO4 | C. | Fe2(SO4)3 | D. | FeCl2 |
5.下列说法正确的是( )
| A. | 溶液都是无色、均一、稳定的液体 | |
| B. | 在水中加入氯化钠可以增强水的导电性 | |
| C. | 用汽油清洗衣服上的油漆发生乳化现象 | |
| D. | 用高锰酸钾制取氧气实验,收集完氧气后先移导管后移酒精灯 |