题目内容
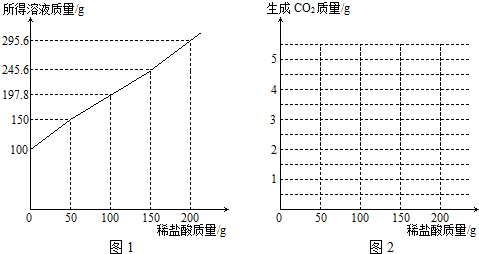
5.工业生产制得的Na2CO3中常含有少量的NaOH.为测定其纯度,某同学取14g样品加水配成100g溶液,慢慢滴入某浓度的稀盐酸,反应所得溶液质量与滴加盐酸的质量关系如图1所示.(1)加入盐酸25g时发生反应的化学方程式NaOH+HCl═NaCl+H2O;
(2)反应过程中共生成CO2的质量是4.4g;
(3)列式计算样品中Na2CO3的质量分数(结果保留0.1%);
(4)在图2中画出生成CO2质量与稀盐酸的质量关系.
分析 (1)根据氢氧化钠钠和盐酸反应生成氯化钠和水解答;
(2)根据质量守恒定律求出二氧化碳的质量解答;
(3)根据碳酸钠和盐酸反应生成氯化钠和水,依据二氧化碳质量计算碳酸钠的质量,进而计算碳酸钠的质量分数.
解答 解:
(1)氢氧化钠钠和盐酸反应生成氯化钠和水,发生反应的化学方程式为:NaOH+HCl═NaCl+H2O;
(2)由图示可知:依据质量守恒定律可知,生成二氧化碳的质量为:150g+150gg-245.6g=4.4g;
(3)设样品中Na2CO3的质量为x.
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 44
x 4.4g
$\frac{106}{x}=\frac{44}{4.4g}$
x=10.6g
样品中Na2CO3的质量分数:$\frac{10.6g}{14g}$×100%=75.7%
(4)在图中画出生成CO2质量与稀盐酸的质量关系为:
答案:
(1)NaOH+HCl═NaCl+H2O;
(2)4.4;
(3)样品中Na2CO3的质量分数为75.7%.
(4)
点评 本题主要考查混合物的有关计算,难度不大,关键是求出二氧化碳的质量.化学变化与数学图形的结合类问题,图形中所出现的拐点为表示恰好完全反应.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
15.实验室有一瓶标签模糊的氢氧化钠溶液,为了测定其溶质质量分数,小明进行了如下实验:
①取一洁净的锥形瓶称量,然后往其中加入一定量的氢氧化钠溶液,并滴入几滴酚酞试液(质量忽略不计),重新称量;
②往上述锥形瓶中加入溶质质量分数为7.3%的盐酸,边加边振荡,溶液红色褪去时,再次称量.数据如下表:
回答下列问题:
(1)若要配制100g 7.3%的盐酸,需要1.1g/cm3 20%的盐酸33.2mL.
(2)根据表中数据,通过计算确定该瓶氢氧化钠溶液的溶质质量分数.(写出计算过程)
(3)小建用pH试纸测得小明实验反应后锥形瓶内溶液的pH为4,则小明测出氢氧化钠溶液的质量分数比实际浓度偏大(选填“偏大”或“偏小”),造成这一偏差的原因是反应后的溶液显酸性,溶液变无色时,滴加盐酸的已过量.
①取一洁净的锥形瓶称量,然后往其中加入一定量的氢氧化钠溶液,并滴入几滴酚酞试液(质量忽略不计),重新称量;
②往上述锥形瓶中加入溶质质量分数为7.3%的盐酸,边加边振荡,溶液红色褪去时,再次称量.数据如下表:
| 锥形瓶/g | 锥形瓶+氢氧化钠溶液/g | 锥形瓶+反应后溶液/g | |
| 质量/g | 35.5 | 60.5 | 110.5 |
(1)若要配制100g 7.3%的盐酸,需要1.1g/cm3 20%的盐酸33.2mL.
(2)根据表中数据,通过计算确定该瓶氢氧化钠溶液的溶质质量分数.(写出计算过程)
(3)小建用pH试纸测得小明实验反应后锥形瓶内溶液的pH为4,则小明测出氢氧化钠溶液的质量分数比实际浓度偏大(选填“偏大”或“偏小”),造成这一偏差的原因是反应后的溶液显酸性,溶液变无色时,滴加盐酸的已过量.
16.下列实验活动不能成功的是( )
| A. | 用熟石灰金别铵态氮肥和钾肥 | B. | 用燃着的木条鉴别氮气和二氧化碳 | ||
| C. | 用灼烧法鉴别羊毛和合成纤维 | D. | 用稀硫酸鉴别黄铜(铜锌合金)和黄金 |
13.下列说法中关于原子的定义正确的是( )
| A. | 原子是构成物质的一种粒子 | B. | 原子质量小、体积小、不断运动 | ||
| C. | 原子是化学变化中的最小粒子 | D. | 原子是由原子核和核外电子构成的 |
10.铁生锈主要条件是( )
| A. | 仅需水 | B. | 仅需氧气 | C. | 水或氧气 | D. | 水和氧气 |
17.二硫基丙醇是医疗上用于治疗砷中毒的药物,化学式为C3H8S2O,可进行肌肉注射或静脉注射.下列关于C3H8S2O的说法正确的是( )
| A. | 二硫基丙醇属于有机化合物 | |
| B. | 二硫基丙醇由碳原子、氢原子、硫原子和氧原子构成 | |
| C. | 二硫基丙醇分子由碳、氢、硫、氧四种元素组成 | |
| D. | 该物质中C3H8S2O元素的质量比为3:8:2:1 |
15.下列物质的性质,前者属于物理性质,后者属于化学性质的是( )
| A. | 活性炭的吸附性 石墨的润滑性 | |
| B. | 甲烷的可燃性 氧气的助燃性 | |
| C. | 浓盐酸的挥发性 碳酸的不稳定性 | |
| D. | 一氧化碳的还原性 金属的导电性 |

 ,上图中与其化学性质相似的元素是C(填序号).
,上图中与其化学性质相似的元素是C(填序号). 某补钙剂说明书的部分信息如图所示,现将有20片该药剂制成的粉末与40g盐酸混合(其他成分不与盐酸反应),恰好完全反应后称得剩余物的质量为55.6g.
某补钙剂说明书的部分信息如图所示,现将有20片该药剂制成的粉末与40g盐酸混合(其他成分不与盐酸反应),恰好完全反应后称得剩余物的质量为55.6g.