题目内容
19.请你根据丙烯胺(C3H5ON),化学式计算后填写(1)丙烯胺(C3H5ON)相对分子质量71
(2)碳元素和氧元素的质量比是9:4
(3)氢元素的质量分数为7%.
分析 (1)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据化合物中元素的质量分数=$\frac{该元素的相对原子质量×原子个数}{该物质相对分子质量}$×100%,进行分析解答.
解答 解:
(1)丙烯酰胺的相对分子质量是12×3+1×5+16+14=71.
(2)丙烯酰胺中碳元素、氧元素的质量比=(12×3):16=9:4.
(3)丙烯酰胺(C3H5ON)中氢元素的质量分数为$\frac{1×5}{71}$×100%≈7%.
故答案为:
(1)71;(2)9:4;(3)7%.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
7.金刚石、石墨和C60的化学性质相似,物理性质却有很大差异.其原因是( )
| A. | 构成它们的原子大小不同 | B. | 构成它们的原子数目不同 | ||
| C. | 三者由不同原子构成 | D. | 它们碳原子的排列方式不同 |
10.下列实验基本操作符合这一要求的是( )
| A. | 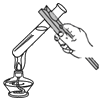 | B. | 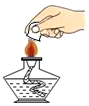 | C. |  | D. | 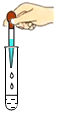 |
14.填写如表:
| 常见的 灭火实例 |  熄灭酒精灯火焰 |  高压水枪喷水灭火 |  防止火势蔓延,将部分树木砍掉 |
| 灭火原理 |
4.化学反应A+B=C+D 中,若agA与一定量的B恰好完全反应,生成mgC和ngD.则参加反应的B的质量为( )
| A. | (m-n)g | B. | (m+n+a)g | C. | (m+n-a)g | D. | (m+n)g |
8. 小红同学进行酸碱中和反应的实验(如图所示),她向氢氧化钠溶液中事先没有滴加指示剂.为了确定盐酸与氢氧化钠溶液中事先没有滴加指示剂,为了确定盐酸与氢氧化钠的反应程度,她从烧杯中取了少量溶液于试管中,并向试管中滴加几滴无色酚酞溶液,振荡,观察到试管中液体颜色没有变化,于是她对烧杯中的溶液进行了以下探究:
小红同学进行酸碱中和反应的实验(如图所示),她向氢氧化钠溶液中事先没有滴加指示剂.为了确定盐酸与氢氧化钠溶液中事先没有滴加指示剂,为了确定盐酸与氢氧化钠的反应程度,她从烧杯中取了少量溶液于试管中,并向试管中滴加几滴无色酚酞溶液,振荡,观察到试管中液体颜色没有变化,于是她对烧杯中的溶液进行了以下探究:
(1)写出盐酸与氢氧化钠溶液反应的化学方程式NaOH+HCl=NaCl+H2O,实验过程中,玻璃棒的作用是搅拌.
(2)小红认为此时烧杯中的溶液可能有以下三种情况:
①盐酸与氢氧化钠溶液恰好完全反应;②氢氧化钠有剩余;③盐酸过量;小明同学却判定不可能“氢氧化钠有剩余”,他的理由是观察到试管中溶液颜色没有变化,说明溶液一定不显碱性,所以不可能是氢氧化钠有剩余.
(3)他们共同设计了一个实验方案,欲对上述其他两种可能情况进行验证,请根据相关内容填写下表:
(4)经过讨论,他们认为利用下列几种物质代替锌粒,也可以达到验证目的,你认为其中不正确的是C(填序号).
A.生锈的铁钉B.碳酸钠粉末C.铜片D.铁片
(5)下列曲线能够表示小红所做实验中溶液pH变化趋势的是C(填序号).

(6)在实验室中,盐酸和氢氧化钠都要密封保存,盐酸需要密封保存的原因是盐酸具有挥发性,氢氧化钠需要密封保存的原因是(用化学方程式表示)2NaOH+CO2=Na2CO3+H2O.
 小红同学进行酸碱中和反应的实验(如图所示),她向氢氧化钠溶液中事先没有滴加指示剂.为了确定盐酸与氢氧化钠溶液中事先没有滴加指示剂,为了确定盐酸与氢氧化钠的反应程度,她从烧杯中取了少量溶液于试管中,并向试管中滴加几滴无色酚酞溶液,振荡,观察到试管中液体颜色没有变化,于是她对烧杯中的溶液进行了以下探究:
小红同学进行酸碱中和反应的实验(如图所示),她向氢氧化钠溶液中事先没有滴加指示剂.为了确定盐酸与氢氧化钠溶液中事先没有滴加指示剂,为了确定盐酸与氢氧化钠的反应程度,她从烧杯中取了少量溶液于试管中,并向试管中滴加几滴无色酚酞溶液,振荡,观察到试管中液体颜色没有变化,于是她对烧杯中的溶液进行了以下探究:(1)写出盐酸与氢氧化钠溶液反应的化学方程式NaOH+HCl=NaCl+H2O,实验过程中,玻璃棒的作用是搅拌.
(2)小红认为此时烧杯中的溶液可能有以下三种情况:
①盐酸与氢氧化钠溶液恰好完全反应;②氢氧化钠有剩余;③盐酸过量;小明同学却判定不可能“氢氧化钠有剩余”,他的理由是观察到试管中溶液颜色没有变化,说明溶液一定不显碱性,所以不可能是氢氧化钠有剩余.
(3)他们共同设计了一个实验方案,欲对上述其他两种可能情况进行验证,请根据相关内容填写下表:
| 实验方法 | 可能观察到的现象 | 结论 |
| 将少量锌粒放入试管中,然后从烧杯中取适量溶液至试管中 | 如果 有气泡产生 | 则盐酸过量,反应的化学方程式是: Zn+2HCl=ZnCl2+H2O |
| 如果 没有气泡产生 | 盐酸和氢氧化钠恰好完全反应 |
A.生锈的铁钉B.碳酸钠粉末C.铜片D.铁片
(5)下列曲线能够表示小红所做实验中溶液pH变化趋势的是C(填序号).

(6)在实验室中,盐酸和氢氧化钠都要密封保存,盐酸需要密封保存的原因是盐酸具有挥发性,氢氧化钠需要密封保存的原因是(用化学方程式表示)2NaOH+CO2=Na2CO3+H2O.
9.下列物质由离子构成的是( )
| A. | 水 | B. | 氯化钠 | C. | 金刚石 | D. | 镁 |
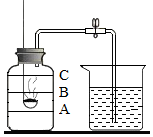 小华为了探究空气的成分,设计了如下实验(如图示):将导管上的弹簧夹夹紧,在燃烧匙中装满红磷,把燃烧匙放在酒精灯火焰上,点燃红磷后,迅速插入集气瓶内,塞紧橡皮塞.小华观察到红磷在瓶内继续燃烧,瓶内充满白烟.待集气瓶冷却到室温,瓶内白烟消失后,发现燃烧匙内红磷有剩余.把导管的另一端插入盛水的烧杯中,打开弹簧夹,水进入集气瓶.
小华为了探究空气的成分,设计了如下实验(如图示):将导管上的弹簧夹夹紧,在燃烧匙中装满红磷,把燃烧匙放在酒精灯火焰上,点燃红磷后,迅速插入集气瓶内,塞紧橡皮塞.小华观察到红磷在瓶内继续燃烧,瓶内充满白烟.待集气瓶冷却到室温,瓶内白烟消失后,发现燃烧匙内红磷有剩余.把导管的另一端插入盛水的烧杯中,打开弹簧夹,水进入集气瓶.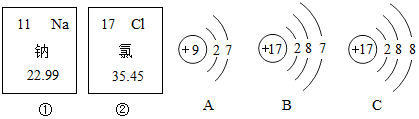
 ;
;