题目内容
10.下列实验基本操作符合这一要求的是( )| A. | 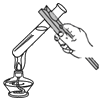 | B. | 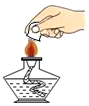 | C. |  | D. | 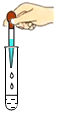 |
分析 A、根据给试管中的液体加热的方法进行分析判断;
B、根据酒精灯的使用方法进行分析判断;
C、根据闻气体气味的方法进行分析判断;
D、根据胶头滴管的使用方法进行分析判断.
解答 解:A、给液体加热时,用酒精灯的外焰加热试管里的液体,且液体体积不能超过试管容积的$\frac{1}{3}$,大拇指要握在试管夹的长柄处,图中所示操作错误;
B、使用酒精灯时要注意“两查、两禁、一不可”,熄灭酒精灯要用灯帽盖灭,图中所示操作正确;
C、闻气体的气味时,防止气体有毒,应用手扇动,不能直接用鼻子闻,图中所示操作错误;
D、向试管中滴加液体的操作要领:试管直立,将胶头滴管垂悬在试管口上方滴加,不能将胶头滴管伸入或接触试管壁,图中所示操作错误.
故选:B.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
相关题目
18.课上,老师展示了一种奇妙的蜡烛,点燃后吹灭又能复燃,请你和他一起探究.
【查阅资料】①普通蜡烛由石蜡和烛芯制成,吹不灭的蜡烛是在烛芯上包裹了少量金属镁粉与稀土元素形成的合金粉末,着火点为150℃,而蜡烛燃烧时温度为550℃-650℃.
②无色酚酞溶液遇碱性物质变红.③Mg(OH)2在热水中微溶,溶液呈碱性.
【探究与思考】
①蜡烛燃烧时,烛芯里的金属不燃烧,为什么?因为蜡烛燃烧时将氧气消耗,烛芯中氧气不足,金属烧不着.
②为什么蜡烛一熄灭,又可以重新燃烧蜡烛一旦熄灭,金属尚未降温至150°C以下,接触到氧气,又可以重新燃.
【科学探究】在老师的引导下,同学们将打磨过的镁条放到装有热的蒸馏水的试管中,发现镁条表面有少量气泡.
(1)提出问题:产生的气体是什么?
(2)猜想与假设:【甲同学猜】H2;【你猜】氧气;【丙同学猜】CO2.乙同学的猜想提出后,其他小组同学纷纷反对,原因是根据质量守恒定律,反应物中没有C元素.
(3)实验与结论:
(4)讨论与交流:正确填写以下内容你将获得激励分4分.
a.因为实验Ⅰ、Ⅱ中产生气体速率慢,不易验证产物,老师提供以下信息:任意化学反应中,有元素化合价升高,必有元素化合价降低,请你结合以上的探究内容和信息,写出镁与水的反应方程式Mg+H2O═Mg(OH)2+H2↑.
b.如图是小莺利用数字实验测定的金属与酸反应时压强的变化曲线,则:

【查阅资料】①普通蜡烛由石蜡和烛芯制成,吹不灭的蜡烛是在烛芯上包裹了少量金属镁粉与稀土元素形成的合金粉末,着火点为150℃,而蜡烛燃烧时温度为550℃-650℃.
②无色酚酞溶液遇碱性物质变红.③Mg(OH)2在热水中微溶,溶液呈碱性.
【探究与思考】
①蜡烛燃烧时,烛芯里的金属不燃烧,为什么?因为蜡烛燃烧时将氧气消耗,烛芯中氧气不足,金属烧不着.
②为什么蜡烛一熄灭,又可以重新燃烧蜡烛一旦熄灭,金属尚未降温至150°C以下,接触到氧气,又可以重新燃.
【科学探究】在老师的引导下,同学们将打磨过的镁条放到装有热的蒸馏水的试管中,发现镁条表面有少量气泡.
(1)提出问题:产生的气体是什么?
(2)猜想与假设:【甲同学猜】H2;【你猜】氧气;【丙同学猜】CO2.乙同学的猜想提出后,其他小组同学纷纷反对,原因是根据质量守恒定律,反应物中没有C元素.
(3)实验与结论:
| 实验 | 操作步骤 | 现象 | 结论 |
| Ⅰ | 往镁与水反应的试管中滴加1-2滴无色酚酞溶液 | 溶液变红色 | 生成了碱[Mg(OH)2] |
| Ⅱ | 加热Ⅰ中的试管 | 产生气体变多 | 温度上升,化学反应速率加快 |
a.因为实验Ⅰ、Ⅱ中产生气体速率慢,不易验证产物,老师提供以下信息:任意化学反应中,有元素化合价升高,必有元素化合价降低,请你结合以上的探究内容和信息,写出镁与水的反应方程式Mg+H2O═Mg(OH)2+H2↑.
b.如图是小莺利用数字实验测定的金属与酸反应时压强的变化曲线,则:

1.为研究锌和铝的金属活动性,某研究小组进行了如下探究.
(1)小明设计的实验方案:向表面积相同的铝片和锌粒中分别加入盐酸.写出锌与盐酸反应的化学方程式:Zn+2HCl═ZnCl2+H2↑.
(2)小芳将去膜和未去膜的铝片分别放入盐酸中,发现前者比后者反应快,原因是未去膜的铝片表面有氧化铝(氧化膜),氧化铝先与盐酸反应.
(3)小芳在(2)实验中,还观察到有“灰黑色沉淀”这一异常现象出现.
【提出问题】铝与盐酸反应出现的灰黑色沉淀的组成是什么?
【查阅文献】铝在颗粒较小时为灰黑色;AlCl3为无色透明晶体或白色而微带浅黄色的固体,易溶于水和乙醇.
【提出合理假设】假设a:该灰黑色沉淀可能含有铝(或铝和氯化铝的混合物);
假设b:该灰黑色沉淀可能含有AlCl3;
假设c:该灰黑色沉淀可能含有难溶于酸的物质.
【设计并完成实验】取灰黑色沉淀分别进行如下实验.
【得出结论】由实验①可判断假设c不成立(填“成立”或“不成立”),再集合②和③可得出该灰黑色沉淀的成分是铝和氯化铝.
(4)你认为(1)小明的实验能否比较锌和铝的金属活动性强弱?不能(填“能”或“不能”),分别从设计方法和操作可行性的角度,具体说明理由:-小明的实验方案中未控制金属的纯度,盐酸的浓度等相关变量相同;操作中难以做到铝片和锌粒的表面积相同.
(1)小明设计的实验方案:向表面积相同的铝片和锌粒中分别加入盐酸.写出锌与盐酸反应的化学方程式:Zn+2HCl═ZnCl2+H2↑.
(2)小芳将去膜和未去膜的铝片分别放入盐酸中,发现前者比后者反应快,原因是未去膜的铝片表面有氧化铝(氧化膜),氧化铝先与盐酸反应.
(3)小芳在(2)实验中,还观察到有“灰黑色沉淀”这一异常现象出现.
【提出问题】铝与盐酸反应出现的灰黑色沉淀的组成是什么?
【查阅文献】铝在颗粒较小时为灰黑色;AlCl3为无色透明晶体或白色而微带浅黄色的固体,易溶于水和乙醇.
【提出合理假设】假设a:该灰黑色沉淀可能含有铝(或铝和氯化铝的混合物);
假设b:该灰黑色沉淀可能含有AlCl3;
假设c:该灰黑色沉淀可能含有难溶于酸的物质.
【设计并完成实验】取灰黑色沉淀分别进行如下实验.
| 实验编号 | 实验操作 | 实验现象 |
| ① | 加入适量稀盐酸 | 有微量气泡,固体全部溶解,得到澄清溶液 |
| ② | 加入适量蒸馏水 | 固体部分溶解 |
| ③ | 加入适量无水乙醇 | 固体部分溶解 |
(4)你认为(1)小明的实验能否比较锌和铝的金属活动性强弱?不能(填“能”或“不能”),分别从设计方法和操作可行性的角度,具体说明理由:-小明的实验方案中未控制金属的纯度,盐酸的浓度等相关变量相同;操作中难以做到铝片和锌粒的表面积相同.
18.某兴趣小组为了探究铝、铁、铜三种金属的活动性,用铜丝、铁丝、铝丝和稀盐酸四种物质,设计了以下只用一只试管、取用一次盐酸的探究方案.请你和他们一起完善表的探究方案并回答有关问题.
结论:金属活动性由强到弱顺序是Al>Fe>Cu.
| 实验步骤 | 观察到的现象 | 化学方程式 |
| ①取适量盐酸于试管中,插入铁丝,充分作用. | 有气泡生成,溶液由无色 变成浅绿色. | Fe+2HCl═FeCl2+H2↑ |
| ②在①所得溶液中,插入 铜丝,充分作用. | 无明显现象 | |
| ③在②所得溶液中,插入 铝丝,充分作用. | 金属表面有一层黑色物质生成 | 2Al+3FeCl2=2AlCl3+3Fe |
5.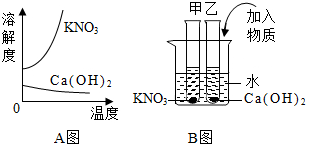 A图表示硝酸钾和氢氧化钙的溶解度随温度变化的情况.B图中甲、乙试管分别盛有硝酸钾、氢氧化钙的饱和溶液,试管底部均有未溶解的固体.向烧杯中加入一种物质后,甲试管中固体减少,乙试管中的固体增加,则加入的物质不可能是( )
A图表示硝酸钾和氢氧化钙的溶解度随温度变化的情况.B图中甲、乙试管分别盛有硝酸钾、氢氧化钙的饱和溶液,试管底部均有未溶解的固体.向烧杯中加入一种物质后,甲试管中固体减少,乙试管中的固体增加,则加入的物质不可能是( )
 A图表示硝酸钾和氢氧化钙的溶解度随温度变化的情况.B图中甲、乙试管分别盛有硝酸钾、氢氧化钙的饱和溶液,试管底部均有未溶解的固体.向烧杯中加入一种物质后,甲试管中固体减少,乙试管中的固体增加,则加入的物质不可能是( )
A图表示硝酸钾和氢氧化钙的溶解度随温度变化的情况.B图中甲、乙试管分别盛有硝酸钾、氢氧化钙的饱和溶液,试管底部均有未溶解的固体.向烧杯中加入一种物质后,甲试管中固体减少,乙试管中的固体增加,则加入的物质不可能是( )| A. | 硝酸铵 | B. | 氢氧化钠 | C. | 生石灰 | D. | 浓硫酸 |
15.某学生量取液体,视线与液体凹液面的最低处相平,读数为30毫升,将液体倒出一部分后,俯视读数为20毫升,则该同学实际倒出的液体体积为( )
| A. | 大于10毫升 | B. | 小于10毫升 | C. | 等于10毫升 | D. | 无法确定 |
2.下列实验操作中,正确的是( )
| A. | 实验剩余的药品应放回原试剂瓶 | |
| B. | 给烧杯加热时,要垫上石棉网 | |
| C. | 加热试管中的固体时试管口略向上倾斜 | |
| D. | 把块状固体投入直立的试管中 |
