题目内容
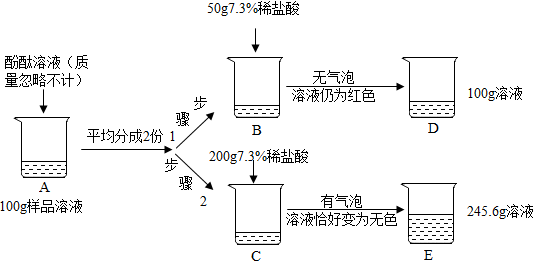
20.将一定质量的石灰石固体放入100g稀盐酸中,恰好完全反应后,溶液的质量增加至105.6g(假设杂质不溶于水且不与稀盐酸反应,气体完全逸出).则:(1)产生二氧化碳的质量是4.4g.
(2)反应后所得溶质的质量分数是多少?
分析 本题根据溶液的质量差量进行求算,因为加入的是碳酸钙,生成的是二氧化碳气体跑掉了,溶液的质量增加就是因为这个碳酸钙和生成的二氧化碳之间的质量差值.
解答 解:设生成的二氧化碳的质量为x,生成的氯化钙的质量为y.
CaCO3+2HCl═CaCl2+H2O+CO2↑ 溶液质量增加
100 111 44 100-44=56
y x 105.6g-100g=5.6g
$\frac{111}{y}$=$\frac{44}{x}$=$\frac{56}{5.6g}$
x=4.4g
y=11.1g
反应后所得溶质的质量分数为$\frac{11.1g}{105.6g}$×100%≈10.5%
答:(1)产生二氧化碳的质量是 4.4g.
(2)反应后所得溶质的质量分数约为10.5%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
相关题目
1. 厨房中的实验室
厨房中的实验室
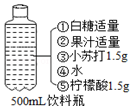
(1)在厨房中可以自制碳酸饮料,配料表如图所示.产生的二氧化碳气体是配料表中的柠檬酸与小苏打反应生成的,人体胃液中的酸也可以与该物质反应,其方程式为NaHCO3+HCl=NaCl+H2O+CO2↑.
(2)紫罗兰的花瓣汁液呈紫色,将它分别滴加到盛有下列溶液的试管中有如下现象:
将紫罗兰花瓣汁液滴入肥皂水中溶液呈蓝色,说明肥皂水显碱性.
 厨房中的实验室
厨房中的实验室(1)在厨房中可以自制碳酸饮料,配料表如图所示.产生的二氧化碳气体是配料表中的柠檬酸与小苏打反应生成的,人体胃液中的酸也可以与该物质反应,其方程式为NaHCO3+HCl=NaCl+H2O+CO2↑.
(2)紫罗兰的花瓣汁液呈紫色,将它分别滴加到盛有下列溶液的试管中有如下现象:
| 溶液名称 | 白醋 | 稀盐酸 | 氯化钠溶液 | 蒸馏水 | 石灰水 | 氢氧化钠溶液 |
| 紫罗兰 | 红色 | 红色 | 紫色 | 紫色 | 蓝色 | 蓝色 |
2.下列物质属下金属材料的是( )
| A. | 钨灯丝 | B. | 铁矿石 | C. | 二氧化锰 | D. | 碳 |
15.煤燃烧产生的废气中含有SO2,SO2溶于水会形成酸雨.用NaOH、Na2SO3溶液可将90%以上的SO2吸收,涉及的反应有:①2NaOH+SO2═Na2SO3+H2O ②Na2SO3+SO2+H2O═2NaHSO3③NaHSO3+NaOH═Na2SO3+H2O.下列说法中错误的是( )
| A. | NaHSO3属于酸 | |
| B. | 吸收SO2的过程中,Na2SO3可循环使用 | |
| C. | 酸雨是指pH<5.6的雨水 | |
| D. | 反应①说明SO2与CO2有相似的化学性质 |
5.将一定质量的a、b、m、n四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得各物质的质量如下:
下列说法错误的是( )
| 物质 | a | b | m | n |
| 反应前的质量/g | 6.4 | 3.2 | 4.0 | 2.5 |
| 反应后的质量/g | 3.8 | 待测数据 | 7.2 | 2.5 |
| A. | a和b是反应物,n可能是催化剂 | |
| B. | 上表中的“待测数据”的数值为0.6 | |
| C. | m物质中所含元素,一定与A、B两种物质中元素相同 | |
| D. | 该反应一定属于化合反应 |
12.PM2.5是指大气中直径小于或等于2.5微米的颗粒物,对人体健康影响很大,主要来源之一是化石燃料.下列措施能减少PM2.5污染的是( )
| A. | 鼓励开私家车出行 | B. | 鼓励用液化石油气作燃料 | ||
| C. | 鼓励用煤火力发电 | D. | 鼓励使用太阳能热水器 |
10.下列反应属于复分解反应的是( )
| A. | S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2 | B. | 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ | ||
| C. | C+2CuO$\frac{\underline{\;高温\;}}{\;}$CO2↑+2Cu | D. | Al(OH)3+3HCl═AlCl3+3H2O |
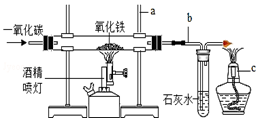 实验室模拟炼铁的实验装置如图所示.
实验室模拟炼铁的实验装置如图所示.