题目内容
2.银铜合金广泛用于航空工业,从切割肥料中回收银并制备铜化工产品的工艺流程如图所示:[已知Al(OH)3和Cu(OH)2开始分解的温度分别为450℃和80℃]
(1)操作Ⅰ和操作Ⅱ的名称为过滤.
(2)步骤①中,在空气中进行熔炼的目的是把铜转化成氧化铜.
(3)步骤②中发生反应的化学方程式为CuO+H2SO4=CuSO4+H2O.
分析 (1)通过过滤能够把固体和液体分离;
(2)步骤①中,在空气中进行熔炼时,铜能和空气中的氧气反应生成氧化铜;
(3)步骤②中,加入稀硫酸时,银不能和稀硫酸反应,氧化铜能和稀硫酸反应生成硫酸铜和水.
解答 解:(1)操作Ⅰ和操作Ⅱ的名称为过滤,通过过滤能够把固体和液体分离.
故填:过滤.
(2)步骤①中,在空气中进行熔炼时,铜能和空气中的氧气反应生成氧化铜,因此在空气中进行熔炼的目的是把铜转化成氧化铜.
故填:把铜转化成氧化铜.
(3)步骤②中,加入稀硫酸时,银不能和稀硫酸反应,氧化铜能和稀硫酸反应生成硫酸铜和水,发生反应的化学方程式为:CuO+H2SO4=CuSO4+H2O.
故填:CuO+H2SO4=CuSO4+H2O.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
3.下列图例中属于“禁止烟火”标志的是( )
| A. |  | B. |  | C. |  | D. |  |
4.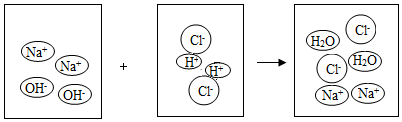 将一定量的氢氧化钠溶液与稀盐酸混合,二者恰好完全反应的微观示意图如下.由此分析下列说法正确的是( )
将一定量的氢氧化钠溶液与稀盐酸混合,二者恰好完全反应的微观示意图如下.由此分析下列说法正确的是( )
 将一定量的氢氧化钠溶液与稀盐酸混合,二者恰好完全反应的微观示意图如下.由此分析下列说法正确的是( )
将一定量的氢氧化钠溶液与稀盐酸混合,二者恰好完全反应的微观示意图如下.由此分析下列说法正确的是( )| A. | 反应前后阴、阳离子的总数目不变 | B. | 反应前后溶剂质量不变 | ||
| C. | 反应后溶液呈中性 | D. | 反应前后元素种类发生了变化 |
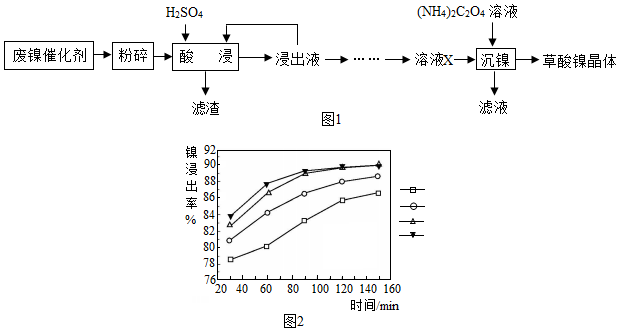
17.草酸镍晶体(NiC2O4•2H2O)可用于制镍催化剂.某小组用废镍催化剂(成分为Fe2O3、Ni、Fe、SiO2等)制备草酸镍晶体的部分实验流程如图1:
已知:①Ni能和稀H2SO4反应.
②相关金属离子生成氢氧化物沉淀的pH如表
③H2O2能将Fe2+氧化为Fe3+
(1)废镍催化剂“粉碎”的目的是增大与硫酸的接触面积,加快反应速率.
(2)保持其他条件相同,在不同温度下对废镍催化剂进行“酸浸”,镍浸出率随时间变化如图2,“酸浸”的适宜温度与时间分别为C(填字母).
A.30℃、30min B.90℃、150min C.70℃、120min D.90℃、120min
(3)“酸浸”中发生的复分解反应方程式为Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
(4)“浸出液”得到“溶液x”过程中,加入试剂先后顺序是A(填字母)
A.先加H2O2溶液,再加NaOH溶液 B.先加NaOH溶液,再加H2O2溶液
加NaOH溶液调节pH3.2~6.7(填范围),充分反应后得到滤渣的操作是过滤,该操作中所用到的玻璃仪器有玻璃棒、烧杯和漏斗.
(5)将“沉镍”工序:①主要过程为:蒸发浓缩、降温结晶、过滤,所得固体用75%乙醇洗涤、110℃下烘干,得草酸镍晶体.
②用75%乙醇洗涤的目的是洗去杂质、减少草酸镍晶体的损失;
③烘干温度不超过110℃的原因是防止草酸镍失去结晶水.

已知:①Ni能和稀H2SO4反应.
②相关金属离子生成氢氧化物沉淀的pH如表
| 金属离子 | 开始沉淀的pH | 完全沉淀的pH |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Ni2+ | 6.7 | 9.5 |
(1)废镍催化剂“粉碎”的目的是增大与硫酸的接触面积,加快反应速率.
(2)保持其他条件相同,在不同温度下对废镍催化剂进行“酸浸”,镍浸出率随时间变化如图2,“酸浸”的适宜温度与时间分别为C(填字母).
A.30℃、30min B.90℃、150min C.70℃、120min D.90℃、120min
(3)“酸浸”中发生的复分解反应方程式为Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
(4)“浸出液”得到“溶液x”过程中,加入试剂先后顺序是A(填字母)
A.先加H2O2溶液,再加NaOH溶液 B.先加NaOH溶液,再加H2O2溶液
加NaOH溶液调节pH3.2~6.7(填范围),充分反应后得到滤渣的操作是过滤,该操作中所用到的玻璃仪器有玻璃棒、烧杯和漏斗.
(5)将“沉镍”工序:①主要过程为:蒸发浓缩、降温结晶、过滤,所得固体用75%乙醇洗涤、110℃下烘干,得草酸镍晶体.
②用75%乙醇洗涤的目的是洗去杂质、减少草酸镍晶体的损失;
③烘干温度不超过110℃的原因是防止草酸镍失去结晶水.
7.正确的化学实验操作,对实验结果、人身安全很重要.下图中的实验操作正确的是( )
| A. |  稀释浓硫酸 | B. |  闻气体 | C. |  移走蒸发皿 | D. |  倒液体 |
11.下列说法正确的是( )
| A. | 等质量的二氧化硫和三氧化硫中硫元素的质量比为5:4 | |
| B. | 等质量的乙醇和甲烷完全燃烧,生成的二氧化碳和水的质量均相等 | |
| C. | 等质量的高锰酸钾和氯酸钾分别受热完全分解,生成氧气质量相等 | |
| D. | 等质量的碳酸钠和碳酸氢钠分别与足量稀盐酸充分反应,生成二氧化碳质量相等 |
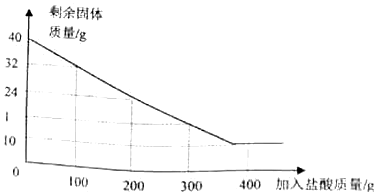
12.生铁是铁和碳的合金,为测定某炼铁厂生产的生铁样品中铁的质量分数,化学兴趣小组的同学称得该生铁样品6.0g,放入烧杯中,向其中加入65.0g稀硫酸,恰好完全反应(Fe+H2SO4═FeSO4+H2↑)(假设杂质不参与反应),测得的实验数据如下:
请你完成有关计算(结果保留一位小数):
(1)硫酸中H:S:O的元素质量比是1:16:24.
(2)反应放出的氢气是0.2g.
(3)生铁样品中铁的质量分数是多少?
(4)反应后所得溶液中溶质的质量分数是多少?
| 反应前 | 反应后 | |
| 烧杯及其中物质的质量 | 97.0g | 96.8g |
(1)硫酸中H:S:O的元素质量比是1:16:24.
(2)反应放出的氢气是0.2g.
(3)生铁样品中铁的质量分数是多少?
(4)反应后所得溶液中溶质的质量分数是多少?