题目内容
11.下列说法正确的是( )| A. | 等质量的二氧化硫和三氧化硫中硫元素的质量比为5:4 | |
| B. | 等质量的乙醇和甲烷完全燃烧,生成的二氧化碳和水的质量均相等 | |
| C. | 等质量的高锰酸钾和氯酸钾分别受热完全分解,生成氧气质量相等 | |
| D. | 等质量的碳酸钠和碳酸氢钠分别与足量稀盐酸充分反应,生成二氧化碳质量相等 |
分析 A、根据二氧化硫和三氧化硫的化学式计算;
B、根据乙醇和甲烷燃烧的化学方程式判断;
C、根据加热高锰酸钾和氯酸钾的化学方程式计算;
D、根据碳酸钠和碳酸氢钠与盐酸反应的化学方程式判断.
解答 解:A、等质量的二氧化硫和三氧化硫中硫元素的质量比为$\frac{32}{64}:\frac{32}{80}=\frac{5}{4}$,正确;
B、CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O
16 44 36
C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O
46 88 54
故等质量的乙醇和甲烷完全燃烧,生成的二氧化碳和水的质量不相等,错误;
C、2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
245 96
2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
316 32
故等质量的高锰酸钾和氯酸钾分别受热完全分解,生成氧气质量不相等,错误;
D、Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 44
NaHCO3+HCl═NaCl+H2O+CO2↑
84 44
故等质量的碳酸钠和碳酸氢钠分别与足量稀盐酸充分反应,生成二氧化碳质量不相等,错误;
故选A.
点评 本题考查的是化学反应中各物质间的质量关系,完成此题,可以依据已有的知识进行.

| A. | 该固体分子在不停运动 | |
| B. | 该固体和水的化学性质相同 | |
| C. | 该固体分子间没有间隔 | |
| D. | 由普通水制得固体发生的是物理变化 |
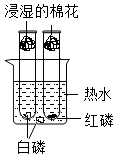 小徐根据如图实验装置进行可燃物燃烧条件的探究,有关该实验和装置的分析合理的是( )
小徐根据如图实验装置进行可燃物燃烧条件的探究,有关该实验和装置的分析合理的是( )| A. | 烧杯中的热水只能起到升高可燃物温度的作用 | |
| B. | 湿棉花的作用是防止空气中的CO2进入试管 | |
| C. | 试管内外的白磷现象不同,因为其着火点不同 | |
| D. | 对实验的分析可以得出可燃物燃烧所需的条件 |
| A. |  过滤 | B. |  滴加液体药品 | ||
| C. |  检查装置的气密性 | D. |  点燃酒精灯 |
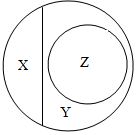 分类是研究物质的常用方法.右图是纯净物、单质、化合物、氧化物之间关系的形象表示,若整个大圈表示纯净物,则下列物质属于Z范围的是( )
分类是研究物质的常用方法.右图是纯净物、单质、化合物、氧化物之间关系的形象表示,若整个大圈表示纯净物,则下列物质属于Z范围的是( )| A. | 红磷 | B. | 干冰 | C. | 氯酸钾 | D. | 食盐水 |
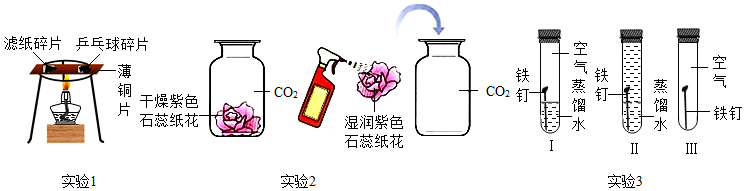

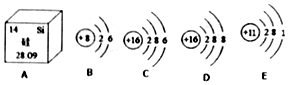 在宏观、微观和符号之间建立联系是化学学科的重要思维方式,根据图中提供的信息,请回答下列问题;
在宏观、微观和符号之间建立联系是化学学科的重要思维方式,根据图中提供的信息,请回答下列问题;