题目内容
14.化学兴趣小组同学为了测定赤铁矿中氧化铁的质量分数,取40g赤铁矿样品放入烧杯中,再取400g稀盐酸分四次加入烧杯中,每次均充分反应(杂质不溶于水,也不参加反应),测得实验数据如图,请计算:(1)此赤铁矿中氧化铁的质量分数75%;
(2)稀盐酸中溶质质量分数.
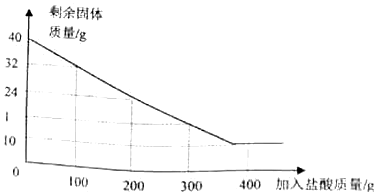
分析 (1)赤铁矿中氧化铁与盐酸反应,杂质不溶于水,也不参加反应,最后剩余的固体质量为杂质;
(2)根据氧化铁的质量结合方程式计算氯化氢的质量,进一步计算稀盐酸中溶质质量分数.
解答 解:(1)最后剩余的固体质量为杂质,40g赤铁矿中氧化铁的质量为40g-10g=30g,
此赤铁矿中氧化铁的质量分数$\frac{30g}{40g}×100%$=75%.
(2)设100g盐酸中HCl质量为x
Fe2O3+6HCl=2FeCl3+3H2O
160 219
8g x
$\frac{160}{8g}=\frac{219}{x}$
x=10.95g
稀盐酸中溶质质量分数为$\frac{10.95g}{100g}×100%$=10.95%
答:盐酸中HCl质量分数为10.95%.
故答案为:(1)75%;(2)盐酸中HCl质量分数为10.95%.
点评 本题难度较大,考查了根据化学方程式的计算,根据图象数据分析出剩余固体是正确解答本题的关键所在.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
19.美国科学家日前利用普通水制得了一种新的固体,该新型固体每个分子由1个氢原子和一个氧原子构成.下列说法正确的是( )
| A. | 该固体分子在不停运动 | |
| B. | 该固体和水的化学性质相同 | |
| C. | 该固体分子间没有间隔 | |
| D. | 由普通水制得固体发生的是物理变化 |
6.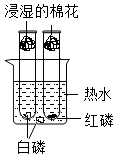 小徐根据如图实验装置进行可燃物燃烧条件的探究,有关该实验和装置的分析合理的是( )
小徐根据如图实验装置进行可燃物燃烧条件的探究,有关该实验和装置的分析合理的是( )
 小徐根据如图实验装置进行可燃物燃烧条件的探究,有关该实验和装置的分析合理的是( )
小徐根据如图实验装置进行可燃物燃烧条件的探究,有关该实验和装置的分析合理的是( )| A. | 烧杯中的热水只能起到升高可燃物温度的作用 | |
| B. | 湿棉花的作用是防止空气中的CO2进入试管 | |
| C. | 试管内外的白磷现象不同,因为其着火点不同 | |
| D. | 对实验的分析可以得出可燃物燃烧所需的条件 |
4.化学与人类生产、生活密切相关,下列应用不涉及化学变化的是( )
| A. | 小苏打用作糕点膨松剂 | B. | 生石灰用作袋装食品干燥剂 | ||
| C. | 肥皂水用来区别硬水、软水 | D. | 活性炭用来去除冰箱内异味 |
 Cl-、
Cl-、 H+、
H+、 Cu2+
Cu2+