题目内容
20.某兴趣小组同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验.请你与他们一起完成以下探究活动:【对固体猜想】猜想I:全部是Na2CO3,猜想的依据是2NaOH+CO2=Na2CO3+H2O(用化学方程式表示)
猜想Ⅱ:全部是NaOH 猜想Ⅲ:部分是NaOH,部分是Na2CO3
【实验和推断】
| 实验步骤 | 实验现象 |
| ①取少量白色固体于试管中,加水振荡后,至全部溶解. | 无色溶液 |
| ②向试管的溶液中滴加适量物质X的溶液 | 现象A |
| ③再向试管中滴加几滴酚酞试液. | 现象B |
(2)若X是Ba(OH)2溶液,现象A为有白色沉淀生成,现象B为无色酚酞试液变红,则该实验不能(填“能”或“不能”)说明样品中有NaOH;
(3)若X是BaCl2溶液(过量),猜想Ⅲ成立的实验现象是现象A有白色沉淀生成,现象B酚酞变红.
分析 【对固体猜想】氢氧化钠和空气中的二氧化钠反应生成碳酸钠和水,所以有三种情况.
【实验和推断】
(1)氢氧化钠变质,就是说生成碳酸钠,碳酸钠和盐酸反应生成氯化钠和水和二氧化碳.
(2)氢氧化钡和碳酸钠反应生成碳酸钡沉淀和氢氧化钠,生成的氢氧化钠能使酚酞变红,因此无法判断原物质中是否有氢氧化钠.
(3)氯化钡和碳酸钠生成碳酸钡和氯化钠,氢氧化钠能使酚酞变红.
解答 解:【对固体猜想】氢氧化钠和空气中的二氧化钠反应生成碳酸钠和水.如果部分参加反应,则最后成分是碳酸钠和氢氧化钠;如果全部参加反应,则最后是碳酸钠.故发生反应的化学方程式为:2NaOH+CO2=Na2CO3+H2O.
【实验和推断】
(1)根据题目信息(氢氧化钠已经变质)可知成分中有碳酸钠.碳酸钠和盐酸生成氯化钠和水和二氧化碳.故答案为:盐酸,Na2CO3+2HCl=2NaCl+H2O+CO2↑.
(2)氢氧化钡和碳酸钠反应生成碳酸钡沉淀和氢氧化钠,生成的氢氧化钠能使酚酞变红,因此无法判断原物质中是否有氢氧化钠.故答案为:不能.
(3)氯化钡和碳酸钠生成碳酸钡和氯化钠,碳酸钡是沉淀,酚酞变红说明含有氢氧化钠.故答案为:现象A有白色沉淀生成,现象B酚酞变红.
故答案为:
【对固体猜想】2NaOH+CO2=Na2CO3+H2O
【实验和推断】(1)盐酸; Na2CO3+2HCl=2NaCl+H2O+CO2↑
(2)不能; (3)现象A有白色沉淀生成,现象B酚酞变红
点评 氢氧化钠易吸水而潮解,然后和二氧化碳反应生成碳酸钠而变质,因此,在探究氢氧化钠变质情况时,需要考虑到碳酸钠溶液对氢氧化钠溶液的影响.在(2)判断是否有氢氧化钠时,一定注意反应产物中的氢氧化钠也可以使酚酞变红,学生要留意.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.氯原子得到1个电子变成氯离子,如图是氯离子的结构示意图,下列叙述正确的是( )
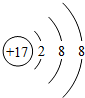
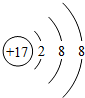
| A. | 氯原子核外有18个电子 | B. | 一个氯离子核内一定有17个质子 | ||
| C. | 氯离子在化学反应中容易得到电子 | D. | 氯元素的相对原子质量是17 |
8.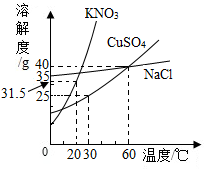 如图是几种盐的溶解度曲线,下列说法正确的是( )
如图是几种盐的溶解度曲线,下列说法正确的是( )
 如图是几种盐的溶解度曲线,下列说法正确的是( )
如图是几种盐的溶解度曲线,下列说法正确的是( )| A. | 40℃时,将35g食盐溶于100g水中,降温至0℃可析出NaCl晶体 | |
| B. | 20℃时,KNO3饱和溶液的质量分数 是31.5% | |
| C. | 60℃时,200g水中溶解80g硫酸铜达饱和,当降温至30℃可析出30g硫酸铜晶体 | |
| D. | 30℃时,将35gNaCl和35gKNO3同时溶于100g水中,蒸发时先析出NaCl |
15.有反应:X+H2SO4═BaSO4↓+2Y,下面分析不正确的是( )
| A. | X可能是BaCl2 | B. | X可能是Ba(NO3)2 | ||
| C. | X和Y的相对分子质量之差为135 | D. | Y中一定含有氢元素 |
5. 食醋是厨房中的一种调味品,其中含有少量醋酸.下列有关醋酸的说法不正确的是( )
食醋是厨房中的一种调味品,其中含有少量醋酸.下列有关醋酸的说法不正确的是( )
 食醋是厨房中的一种调味品,其中含有少量醋酸.下列有关醋酸的说法不正确的是( )
食醋是厨房中的一种调味品,其中含有少量醋酸.下列有关醋酸的说法不正确的是( )| A. | 醋酸分子是由碳、氢、氧三种原子构成的 | |
| B. | 醋酸中碳元素的质量分数为40% | |
| C. | 醋酸是由碳、氢、氧三种元素组成的 | |
| D. | 每个醋酸分子中有8个电子 |
10.如图是A、B、C三种固体溶质(均不含结晶水)的溶解度曲线,根据图示,下列说法不正确的是
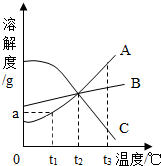

| A. | t1℃时,取50gA的饱和溶液,将温度升高到t2℃,此时溶液中A的质量分数不变(假设升温时,溶剂没有损失) | |
| B. | t1℃,将A、B、C各ag放入100g水中,充分搅拌,所得溶液溶质质量分数均相等 | |
| C. | t3℃时,取相同质量的A、B、C三种饱和溶液降温到t1℃,析出晶体最多的是A | |
| D. | 从A与少量C的混合物中提纯A,可用蒸发结晶的方法 |