题目内容
11.氯原子得到1个电子变成氯离子,如图是氯离子的结构示意图,下列叙述正确的是( )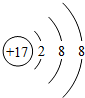
| A. | 氯原子核外有18个电子 | B. | 一个氯离子核内一定有17个质子 | ||
| C. | 氯离子在化学反应中容易得到电子 | D. | 氯元素的相对原子质量是17 |
分析 依据氯离子结构示意图的意义以及最外层电子数的特点分析解答.
解答 解:A、根据氯离子的结构示意图可知该离子的核外电子数是18,氯离子带一个单位的负电荷,所以其核外的电子数比原子多一个电子,所以氯原子核外有17个电子,故A错误;
B、根据氯离子的结构示意图可知一个氯离子核内一定有17个质子,故B正确;
C、氯离子最外层电子数为8,属于稳定结构,所以在化学反应中不容易得到电子,故C错误;
D、根据氯离子的结构示意图不能知道氯元素的相对原子质量,故D错误.
故选B.
点评 要理解和熟记原子结构示意图与离子结构示意图及其含义,根据所给的问题情景或图表信息等,结合所学的相关知识和技能,细致地分析题意,解答即可.

练习册系列答案
 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
1.以下生产、生活中的做法不符合环保理念的是( )
| A. | 开发新能源 | B. | 工业用水重复使用 | ||
| C. | 不露天焚烧秸秆 | D. | 电脑长期处于待机状态 |
16.下列实验操作正确的是( )
| A. |  点燃酒精灯 | B. |  取用粉末状药品 | C. |  收集二氧化碳 | D. |  浓硫酸稀释 |
20.某兴趣小组同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验.请你与他们一起完成以下探究活动:
【对固体猜想】猜想I:全部是Na2CO3,猜想的依据是2NaOH+CO2=Na2CO3+H2O(用化学方程式表示)
猜想Ⅱ:全部是NaOH 猜想Ⅲ:部分是NaOH,部分是Na2CO3
【实验和推断】
(1)若现象A为有气泡产生,则加入的X溶液是盐酸(填溶液名称),说明氢氧化钠已经变质,有气泡产生的反应的化学方程式是Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(2)若X是Ba(OH)2溶液,现象A为有白色沉淀生成,现象B为无色酚酞试液变红,则该实验不能(填“能”或“不能”)说明样品中有NaOH;
(3)若X是BaCl2溶液(过量),猜想Ⅲ成立的实验现象是现象A有白色沉淀生成,现象B酚酞变红.
【对固体猜想】猜想I:全部是Na2CO3,猜想的依据是2NaOH+CO2=Na2CO3+H2O(用化学方程式表示)
猜想Ⅱ:全部是NaOH 猜想Ⅲ:部分是NaOH,部分是Na2CO3
【实验和推断】
| 实验步骤 | 实验现象 |
| ①取少量白色固体于试管中,加水振荡后,至全部溶解. | 无色溶液 |
| ②向试管的溶液中滴加适量物质X的溶液 | 现象A |
| ③再向试管中滴加几滴酚酞试液. | 现象B |
(2)若X是Ba(OH)2溶液,现象A为有白色沉淀生成,现象B为无色酚酞试液变红,则该实验不能(填“能”或“不能”)说明样品中有NaOH;
(3)若X是BaCl2溶液(过量),猜想Ⅲ成立的实验现象是现象A有白色沉淀生成,现象B酚酞变红.
 已知甲、乙、丙为三种不同的单质,A、B、C为三种不同的氧化物.其中A为黑色粉末,B为主要的温室气体,乙为使用最广泛的金属.请回答:
已知甲、乙、丙为三种不同的单质,A、B、C为三种不同的氧化物.其中A为黑色粉末,B为主要的温室气体,乙为使用最广泛的金属.请回答: