题目内容
16.向100g水中不断加入固体A或改变温度,如表所示,得到相应的溶液①~⑤.$\begin{array}{l}{25℃}\\{100g水}\end{array}$ $→_{37.2g}^{加入A}$①$→_{4.2g}^{加入A}$②$→_{至60℃}^{升温}$③$→_{9g}^{加入A}$④$→_{至50℃}^{降}$⑤| 资料:A的溶解度 | |||||
| 温度/℃ | 20 | 30 | 40 | 50 | 60 |
| 溶解/g | 37.2 | 41.4 | 45.8 | 54.4 | 55 |
(2)5个烧杯中溶液的溶质质量分数由小到大的顺序是①<②=③<⑤<④..
分析 根据固体的溶解度表可知:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:A物质在20℃是的溶解度使37.2g,在25℃时的溶解度是41.4g,所以25℃时的溶解度大于37.2g,小于41.4g,①是不饱和溶液,溶质质量分数为:$\frac{37.2g}{137.2g}$×100%=27.1%;
加入4.2g固体A,溶质变成41.4g,所以②是饱和溶液,溶质质量分数为:$\frac{41.4g}{141.4g}$×100%=29.3%;
升温到60℃,溶解度为55.2g,所以③是不饱和溶液,溶质质量分数为:$\frac{41.4g}{141.4g}$×100%=29.3%;
加入9gA,固体变成50.4g,所以④是不饱和溶液,溶质质量分数为:$\frac{50.4g}{150.4g}$×100%=33.5%;
降温到50℃,溶解度为45.8g,所以⑤是饱和溶液,溶质质量分数为:$\frac{45.8g}{145.8g}$×100%=31.4%,所以
(1)属于饱和溶液的是溶液②⑤;
(2)溶液的溶质质量分数从小到大的顺序是:①<②=③<⑤<④.
故答案为:(1)②⑤;
(2):①<②=③<⑤<④.
点评 本题主要考查了饱和溶液和不饱和溶液的判断方法和溶质质量分数的计算,难度不大,需要在平时的学习中加强记忆即可完成.

练习册系列答案
相关题目
7.下列实验操作正确的是( )
| A. |  CO2验满 | B. |  收集O2 | C. |  滴加液体 | D. |  测溶液pH |
4.小刘同学需配制100g10%的氢氧化钠溶液,在配制溶液过程中下列说法正确的是( )
| A. | 在托盘上垫上纸并称取10g氢氧化钠固体 | |
| B. | 用100mL量筒量取90mL水 | |
| C. | 称量时发现指针向右偏转,应调节游码使天平平衡 | |
| D. | 把称取氢氧化钠固体直接倒入装有90mL水的量筒中溶解 |
11.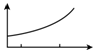 已知浓硫酸敞口放置在空气中,会吸收空气中的水分.某同学通过实验测定了浓硫酸的吸水性的有关数据,绘制成了如图所示的图象.其中横坐标表示时间,那么纵坐标表示的可能是( )
已知浓硫酸敞口放置在空气中,会吸收空气中的水分.某同学通过实验测定了浓硫酸的吸水性的有关数据,绘制成了如图所示的图象.其中横坐标表示时间,那么纵坐标表示的可能是( )
①溶质的质量分数 ②溶剂的质量 ③溶液的质量 ④溶质的质量.
 已知浓硫酸敞口放置在空气中,会吸收空气中的水分.某同学通过实验测定了浓硫酸的吸水性的有关数据,绘制成了如图所示的图象.其中横坐标表示时间,那么纵坐标表示的可能是( )
已知浓硫酸敞口放置在空气中,会吸收空气中的水分.某同学通过实验测定了浓硫酸的吸水性的有关数据,绘制成了如图所示的图象.其中横坐标表示时间,那么纵坐标表示的可能是( )①溶质的质量分数 ②溶剂的质量 ③溶液的质量 ④溶质的质量.
| A. | ①② | B. | ①④ | C. | ②④ | D. | ②③ |
1.在20℃时,把13.6克氯化钾放入40克水中,完全溶解后溶液恰好达到饱和,则该温度下,氯化钾的溶解度是多少( )
| A. | 136克 | B. | 13.6克 | C. | 34克 | D. | 30克 |
6.如图是四位同学的讨论,其中错误的是( )
| A. |  | B. |  | ||
| C. |  | D. |  |
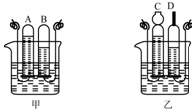 如图甲所示的是电解水实验装置,通电一段时间后,在两个试管中分别收集到气体A和气体B.请回答:
如图甲所示的是电解水实验装置,通电一段时间后,在两个试管中分别收集到气体A和气体B.请回答: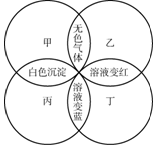 甲、乙、丙、丁分别是紫色石蕊试液、稀硫酸、碳酸钠溶液、澄清石灰水中的一种,若用四个圆表示四种溶液,两圆相交部分为两溶液混合后出现的主要实验现象如图所示.
甲、乙、丙、丁分别是紫色石蕊试液、稀硫酸、碳酸钠溶液、澄清石灰水中的一种,若用四个圆表示四种溶液,两圆相交部分为两溶液混合后出现的主要实验现象如图所示.