题目内容
11.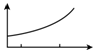 已知浓硫酸敞口放置在空气中,会吸收空气中的水分.某同学通过实验测定了浓硫酸的吸水性的有关数据,绘制成了如图所示的图象.其中横坐标表示时间,那么纵坐标表示的可能是( )
已知浓硫酸敞口放置在空气中,会吸收空气中的水分.某同学通过实验测定了浓硫酸的吸水性的有关数据,绘制成了如图所示的图象.其中横坐标表示时间,那么纵坐标表示的可能是( )①溶质的质量分数 ②溶剂的质量 ③溶液的质量 ④溶质的质量.
| A. | ①② | B. | ①④ | C. | ②④ | D. | ②③ |
分析 溶质质量=溶液质量×溶质质量分数.
解答 解:①随着浓硫酸不断吸收水,溶液质量不断增大,而溶质质量不变,因此溶质的质量分数不断减小;
②随着浓硫酸不断吸收水,溶剂的质量不断增大;
③随着浓硫酸不断吸收水,溶液质量不断增大;
④溶质的质量始终不变;
由以上分析可知,②③.
故选:D.
点评 本题主要考查溶质质量、溶剂质量、溶液质量及其溶质质量分数方面的问题,比较简单.

练习册系列答案
相关题目
1.下列关于青蒿素的说法正确的是( )
| A. | 青蒿素的相对分子质量为282克 | |
| B. | 青蒿素中氧元素的质量分数为11.9% | |
| C. | 青蒿素中C、H、O三种元素的质量比为90:11:40 | |
| D. | 青蒿素由15个碳原子、22个氢原子和5个氧原子构成 |
19.粗盐在制精盐过程中都要用到玻璃棒,玻璃棒在实验中的作用时( )
| A. | 加速粗盐的溶解 | B. | 引流 | C. | 防止液滴飞溅 | D. | 上述3点都是 |
6.下列有关溶液的说法中,正确的是( )
| A. | 不饱和溶液转化为饱和溶液,溶液中溶质的质量分数一定增大 | |
| B. | 将一定质量某物质的饱和溶液降温析出晶体后,所得溶液中溶质的质量一定减小 | |
| C. | 升高温度,饱和溶液一定可以变为不饱和溶液 | |
| D. | 饱和溶液是指不能再溶解任何物质的溶液 |
16.向100g水中不断加入固体A或改变温度,如表所示,得到相应的溶液①~⑤.$\begin{array}{l}{25℃}\\{100g水}\end{array}$ $→_{37.2g}^{加入A}$①$→_{4.2g}^{加入A}$②$→_{至60℃}^{升温}$③$→_{9g}^{加入A}$④$→_{至50℃}^{降}$⑤
(1)②⑤(填序号,下同)中盛的是饱和溶液;
(2)5个烧杯中溶液的溶质质量分数由小到大的顺序是①<②=③<⑤<④..
| 资料:A的溶解度 | |||||
| 温度/℃ | 20 | 30 | 40 | 50 | 60 |
| 溶解/g | 37.2 | 41.4 | 45.8 | 54.4 | 55 |
(2)5个烧杯中溶液的溶质质量分数由小到大的顺序是①<②=③<⑤<④..
3.20℃时,将等质量a、b两种不含结晶水的固体物质,分别加入到盛有100g水的烧杯中,充分搅拌后,现象如图1;然后升温到50℃时,现象如图2;a、b两物质的溶解度曲线如图丙.由这一过程可知( )
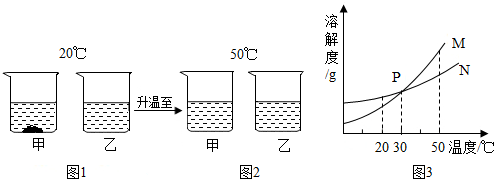

| A. | 30℃时a、b溶液质质量分数不相等 | B. | 图1中a溶液质质量分数比b溶液大 | ||
| C. | 图3中表示a的溶解度曲线是M | D. | 图2中a、b溶液一定都是饱和溶液 |
20.下列叙述正确的是( )
| A. | 浓盐酸溶液和浓硫酸敞口放置一段时间,前者质量分数变小,后者质量分数变大 | |
| B. | 烧碱溶液和石灰水敞口放置一段时间,两者溶液质量均增大,pH值减小 | |
| C. | 稀盐酸中滴入硝酸银,氢氧化钠溶液中滴入氯化镁,直到都恰好反应.则前者溶液pH减小,后者溶液pH增大 | |
| D. | 烧碱固体和纯碱晶体暴露在空气中,前者会潮解导致质量增大,后者会风化导致质量变小 |