题目内容
19.有一包白色粉末可能由NaOH、Na2SO4、CuSO4、Na2CO3和BaCl2中的几种组成,为确定其成分,现做如下实验:①取适量该粉末于试管,加足量的水溶解.过滤,得到沉淀和无色溶液.
②向沉淀中加入过量稀硝酸,沉淀部分溶解且无气泡产生.
则原粉末中一定有氢氧化钠、硫酸铜、氯化钡;一定没有碳酸钠;②中沉淀溶解的化学方程式为Cu(OH)2+2HNO3=Cu(NO3)2+2H2O;①中无色溶液中一定含有的溶质是氯化钠.
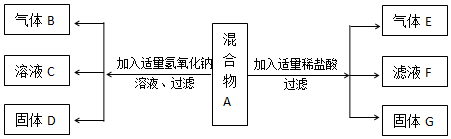
③为证明可能存在的物质是否一定存在,另取①中沉淀5.64g做如下实验:
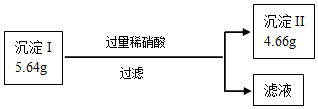
请根据以上数据分析,该物质C存在.
A、一定 B、一定不 C、无法确定.
分析 根据硫酸铜和氢氧化钠反应会生成溶于酸的氢氧化铜沉淀,碳酸钠和氯化钡反应生成碳酸钡沉淀和酸反应会生成二氧化碳气体,硫酸根离子和钡离子反应生成不溶于酸的硫酸钡沉淀等知识进行分析.
解答 解:硫酸铜和氢氧化钠反应会生成溶于酸的氢氧化铜沉淀,碳酸钠和氯化钡反应生成碳酸钡沉淀和酸反应会生成二氧化碳气体,硫酸根离子和钡离子反应生成不溶于酸的硫酸钡沉淀,所以
①取适量该粉末于试管,加足量的水溶解.过滤,得到沉淀和无色溶液,
②向沉淀中加入过量稀硝酸,沉淀部分溶解且无气泡产生,
所以粉末中一定不含碳酸钠,一定含有氯化钡、氢氧化钠、硫酸铜,硫酸铜中也会提供硫酸根离子,所以不能确定是否含有硫酸钠,所以
原粉末中一定有氢氧化钠、硫酸铜、氯化钡,一定没有碳酸钠,②中沉淀溶解的反应是氢氧化铜和硝酸反应生成硝酸铜和水,化学方程式为:Cu(OH)2+2HNO3=Cu(NO3)2+2H2O,①中无色溶液中一定含有的溶质是氯化钠;
另取①中沉淀5.64g做如下实验,加入过量的稀硝酸,得到沉淀4.66g,溶解的氢氧化铜沉淀质量是0.98g,没有样品的质量,所以不能判断样品中是否含有硫酸钠,故选:C.
故答案为:氢氧化钠、硫酸铜、氯化钡,碳酸钠,Cu(OH)2+2HNO3=Cu(NO3)2+2H2O,氯化钠;C.
点评 在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.下列化学用语与其所表达的意义一致的是( )
| A. | N2--2个氮原子 | B. | 3CO--3个一氧化碳分子 | ||
| C. | 3${SO}_{4}^{2-}$--3个硫酸分子 | D. | 2Fe2+--2个铁离子 |
4.如图为某化学反应的微观示意图,下列有关说法中,不正确的是( )

| A. | 该反应属于置换反应 | |
| B. | 反应前后原子的种类、数目均未改变 | |
| C. | 反应前后有两种元素的化合价发生了变化 | |
| D. | 反应中两种单质的质量比为3:2 |