题目内容
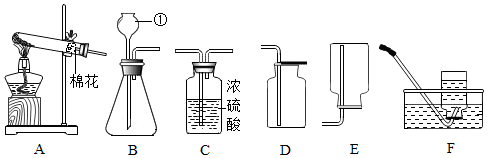
14.如图是实验室制取气体的常用装置.请回答下列问题: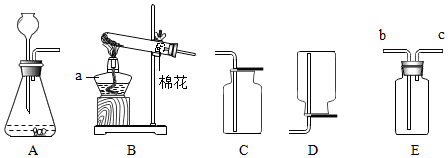
(1)写出图中标号a的仪器名称:酒精灯.
(2)气体的性质是选择气体收集方法的主要依据.下列性质与收集方法的选择无关的是a(填序号)a.颜色b.密度c.溶解性d.与氧气是否反应
(3)实验室制取二氧化碳的反应化学方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑;可选择C(填字母标号)装置收集二氧化碳;若用A装置作发生装置,可能造成的后果是收集不到二氧化碳气体.
(4)用B装置制取氧气的反应化学方程式:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;若用E装置采用排水法收集氧气,气体应从c(填b或c)进入,检验氧气的方法是将带火星的木条伸入集气瓶内,带火星的木条复燃,瓶内是氧气.
(5)为验证CO2气体中含有CO,某同学设计了如下图所示装置,并通过实验验证了CO2气体中含有CO.根据图示回答下列问题.
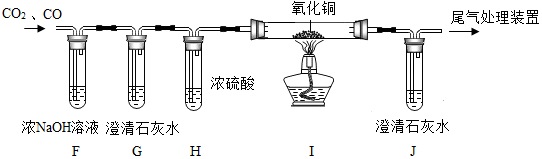
①装置G的作用是检验二氧化碳是否除尽;
②I装置玻璃管中观察到的实验现象是黑色固体逐渐变为红色.
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据收集气体主要有排气法和排水法或排液法,排气法需要比较气体密度大小,是否和空气中的成分发生反应,排水法或排液法需要气体不能和水反应不能易溶于水进行分析;
(3)根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,二氧化碳的密度比空气大,溶于水,用A装置作发生装置制取二氧化碳,生成的二氧化碳会从长颈漏斗逸出进行分析;
(4)根据高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,氧气密度比水小,不易溶于水,氧气有助燃性进行分析;
(5)根据二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,一氧化碳和氧化铜在加热的条件下生成铜和二氧化碳进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,a是酒精灯;
(2)收集气体主要有排气法和排水法或排液法,排气法需要比较气体密度大小,是否和空气中的成分发生反应,排水法或排液法需要气体不能和水反应不能易溶于水,与收集方法的选择无关的是颜色,故选:a;
(3)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑,二氧化碳的密度比空气大,溶于水,所以可选择C装置收集二氧化碳,用A装置作发生装置制取二氧化碳,生成的二氧化碳会从长颈漏斗逸出,所以用A装置作发生装置,可能造成的后果是:收集不到二氧化碳气体;
(4)高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,氧气密度比水小,不易溶于水,氧气有助燃性,所以用E装置采用排水法收集氧气,气体应从c进入,检验氧气的方法是将带火星的木条伸入集气瓶内,带火星的木条复燃,瓶内是氧气;
(5)二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,一氧化碳和氧化铜在加热的条件下生成铜和二氧化碳,所以
①装置G的作用是:检验二氧化碳是否除尽;
②I装置玻璃管中观察到的实验现象是:黑色固体逐渐变为红色.
故答案为:(1)酒精灯;
(2)a;
(3)CaCO3+2HCl=CaCl2+H2O+CO2↑,C,收集不到二氧化碳气体;
(4)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,c,将带火星的木条伸入集气瓶内,带火星的木条复燃,瓶内是氧气;
(5)①检验二氧化碳是否除尽;
②黑色固体逐渐变为红色.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案| A. | 随手关闭水龙头 | B. | 往河流里倾倒垃圾 | ||
| C. | 农业上采用滴灌技术 | D. | 工业废水经处理达标后排放 |
| A. | 除去CO2中混有的HCl:将气体通入NaOH溶液并干燥 | |
| B. | 除去Fe粉中混有的Cu粉:加入过量的CuSO4溶液并干燥 | |
| C. | 除去MnO2中混有的KCl:加入足量的水,过滤后烘干所得固体 | |
| D. | 除去NaCl中混有的Na2CO3:加入适量的稀硝酸溶液 |
| A. | 1个维生素C分子由6个碳原子,8个氢原子,6个氧原子构成 | |
| B. | 维生素C的相对分子质量为176 | |
| C. | 维生素C中C、H、O三种元素的质量比为3﹕4﹕3 | |
| D. | 维生素C中氢元素的质量分数约为4.5% |
 已知:Na2CO3+H2O+CO2═2NaHCO3.如图表示将CO2气体缓慢通入到一定质量的碳酸钠溶液的过程中,某变量y随时间的变化趋势.纵坐标表示的是( )
已知:Na2CO3+H2O+CO2═2NaHCO3.如图表示将CO2气体缓慢通入到一定质量的碳酸钠溶液的过程中,某变量y随时间的变化趋势.纵坐标表示的是( )| A. | 溶液中碳元素的质量 | B. | 碳酸钠的质量分数 | ||
| C. | 溶剂的质量 | D. | 溶液中钠元素的质量 |