题目内容
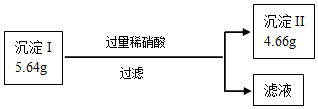
11.某固体混合物A中可能含有Fe、CuO、CaCO3、NH4NO3四种物质中的一种或多种,按图所示进行实验,(设过程中所有可能发生的反应均恰好完全反应)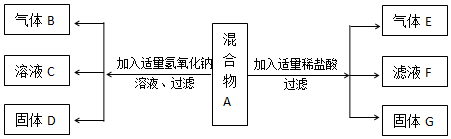
(1)将气体B通入紫色石蕊试液中,试液显蓝 色
(2)固体G中的物质是Cu(写化学式),滤液F中,一定含有的阳离子有2 种(不考虑H+)
(3)固体混合物中,一定含有Fe、CuO、NH4NO3 (写化学式)
(4)混合物A中加入NaOH溶液时,一定发生反应的方程式NH4NO3+NaOH=NaNO3+H2O+NH3↑
(5)该固体混合物A中不能确定的物质是CaCO3(写化学式),若想判断该物质是否存在,可用固体D再进行实验,请简述实验方案(操作现象结论)加入足量的稀盐酸,将生成的气体通入澄清石灰水中,溶液变浑浊,证明含有碳酸钙.
分析 根据铵态氮肥和碱混合会生成氨气,碳酸钙难溶于水,硫酸和氧化铜反应会生成硫酸铜和水,硫酸和铁反应会生成硫酸亚铁和氢气,铁会与硫酸铜反应生成硫酸亚铁和铜,硫酸也会与碳酸钙反应生成二氧化碳气体等知识进行分析.
解答 解:铵态氮肥和碱混合会生成氨气,碳酸钙难溶于水,硫酸和氧化铜反应会生成硫酸铜和水,硫酸和铁反应会生成硫酸亚铁和氢气,铁会与硫酸铜反应生成硫酸亚铁和铜,硫酸也会与碳酸钙反应生成二氧化碳气体,所以
固体混合物A中加入适量的氢氧化钠,会生成气体B,所以A中一定含有硝酸铵,可能含有氧化铜、铁、碳酸钙中的一种或多种;加入适量的稀硫酸,会得到固体G,所以A中一定含有氧化铜、铁,不能确定是否含有碳酸钙,所以
(1)硝酸铵和氢氧化钠反应会生成氨气,所以将气体B通入紫色石蕊试液中,试液显蓝色;
(2)通过推导可知,固体G中的物质是Cu,滤液F中,一定含有的阳离子是亚铁离子和铵根离子2种;
(3)固体混合物中,一定含有Fe、CuO、NH4NO3;
(4)混合物A中加入NaOH溶液时,一定发生的反应是氢氧化钠和硝酸铵反应生成硝酸钠、水和氨气,化学方程式为:NH4NO3+NaOH=NaNO3+H2O+NH3↑;
(5)该固体混合物A中不能确定的物质是:CaCO3,若想判断该物质是否存在,可用固体D再进行实验,实验方案为:加入足量的稀盐酸,将生成的气体通入澄清石灰水中,溶液变浑浊,证明含有碳酸钙.
故答案为:(1)蓝;
(2)Cu,2;
(3)Fe、CuO、NH4NO3;
(4)NH4NO3+NaOH=NaNO3+H2O+NH3↑;
(5)CaCO3,加入足量的稀盐酸,将生成的气体通入澄清石灰水中,溶液变浑浊,证明含有碳酸钙.
点评 在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可.

| A. | 发出明亮的蓝紫色火焰 | |
| B. | 各物质之间的质量比为1:1:1 | |
| C. | 实验前集气瓶底部放少量水 | |
| D. | 该反应用方程式表示为:S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2 |
| A. | 随手关闭水龙头 | B. | 往河流里倾倒垃圾 | ||
| C. | 农业上采用滴灌技术 | D. | 工业废水经处理达标后排放 |
| A. | 除去CO2中混有的HCl:将气体通入NaOH溶液并干燥 | |
| B. | 除去Fe粉中混有的Cu粉:加入过量的CuSO4溶液并干燥 | |
| C. | 除去MnO2中混有的KCl:加入足量的水,过滤后烘干所得固体 | |
| D. | 除去NaCl中混有的Na2CO3:加入适量的稀硝酸溶液 |
| A. | 1个维生素C分子由6个碳原子,8个氢原子,6个氧原子构成 | |
| B. | 维生素C的相对分子质量为176 | |
| C. | 维生素C中C、H、O三种元素的质量比为3﹕4﹕3 | |
| D. | 维生素C中氢元素的质量分数约为4.5% |