题目内容
18.某废旧金属中含有铜、金(Au)和镍(Ni),回收Au并制备CuSO4•5H2O晶体的流程如下: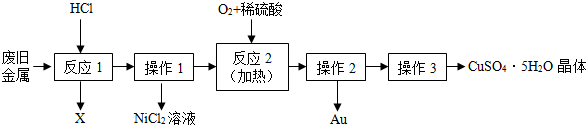
下列说法正确的是( )
| A. | 反应1的生成物为H2O | |
| B. | 操作1和操作2用到玻璃仪器为漏斗、烧杯和玻璃棒 | |
| C. | 三种金属的金属活动性顺序为:Cu>Ni>Au | |
| D. | 反应2的化学方程式为:2Cu+O2+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2CuSO4+2H2O |
分析 根据回收Au并制备CuSO4•5H2O晶体的流程,分析发生的反应,判断金属的活动性顺序.
解答 解:A、由反应的流程图可知,反应1是盐酸与镍反应生成了NiCl2和氢气,没有H2O生成,故A错误;
B、由反应的流程图可知,操作1和操作2都是固体和液体分离,都是过滤,用到玻璃仪器为漏斗、烧杯和玻璃棒.故B正确;
C、由于镍能与盐酸反应,位于氢的前边,所以三种金属的金属活动性顺序为:Ni>Cu>Au,故错误;
D、由反应的流程图可知,反应2的化学方程式为:2Cu+O2+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2CuSO4+2H2O,故D正确.
故选BD.
点评 本题考查了从废旧金属中回收金属或制取某种物质的反应,完成此题,可以依据金属活动性顺序及其意义以及过滤的原理和操作进行解答即可.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案
相关题目
8.下列不能由金属和酸直接反应得到的物质是( )
| A. | 硫酸铜 | B. | 硫酸锌 | C. | 氯化亚铁 | D. | 氯化镁 |
6.下列实验操作正确的是( )
| A. | 排水法收集氧气时,当导管口能开始有气泡冒出时立即收集,防止气体逃逸 | |
| B. | 稀释浓硫酸时,沿烧杯壁将水缓缓注入盛有浓硫酸的烧杯中,并用玻璃棒不断搅拌 | |
| C. | 过滤时,用玻璃棒在过滤器中不断搅拌 | |
| D. | 氢气、一氧化碳等可燃性气体点燃前进行验纯 |
13.下列化学知识的归纳,有错误的一组是( )
| A.实验仪器的使用 | B.自来水的生产 |
| 烧杯加热--应垫石棉网加热 洗净的试管--管口向上正放在试管架上 | 混凝剂--吸附水中悬浮颗粒沉降除去 消毒剂--除去水中的细菌 |
| C.化学与生活 | D.重要化学史 |
| 墙内开花墙外香--分子在不停运动 打开瓶盖,汽水喷出--气体溶解度随压强减小而减小 | 拉瓦锡--通过实验研究空气成分 居里夫妇--发现放射性元素钋和镭 |
| A. | A | B. | B | C. | C | D. | D |
10.2015年“世界水日”、“中国水周”的宣传主题为“节约水资源,保障水安全”.下列有关水的认识中正确的是( )
| A. | 明矾可以区分硬水和软水 | |
| B. | 在自来水厂净化水的过程中,发生的变化都是物理变化 | |
| C. | 水体有自净能力,未经处理的生活污水可任意排放 | |
| D. | 农业生活中改变灌溉方式,变漫灌为喷灌或滴灌,以节约用水 |
8.学习化学的一个重要途径是科学探究,我们做化学实验是科学探究的重要手段,下列化学实验操作不正确的是( )
| A. |  倾倒液体 | B. |  熄灭酒精灯 | C. |  读取液体的体积 | D. |  闻气体的气味 |