题目内容
7.过氧化钠(Na2O2)是一种黄色固体.某次科技活动中,某化学兴趣小组的同学将包有Na2O2固体的棉花放入图1烧杯中,缓慢倒入CO2后发现处于下位的蜡烛先熄灭,上位的后熄灭,同时又惊奇的发现棉花燃烧起来.I.实验过程中“下位的蜡烛先熄灭,上位的后熄灭”的现象说明二氧化碳具有的性质有密度比空气大、不可燃烧且不支持燃烧.
Ⅱ.棉花为什么会燃烧呢?小组同学联想起物质燃烧的相关知识,推理出棉花要燃烧,除了我们已知“棉花是可燃物”之外,还需满足的条件为与氧气接触、温度达到着火点.
提出问题:在实验中是如何给棉花燃烧提供上述条件的呢?
查阅资料:1、2Na2O2+2CO2═Na2CO3+O2↑; 2Na2O2+2H2O═4NaOH+O2↑
2、浓硫酸有吸水性,无水硫酸铜遇水白色会变成蓝色.
设计实验:经过讨论后,小组同学设计了如图2的实验进行探究.
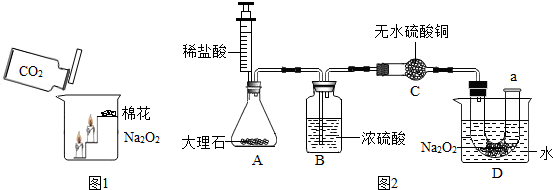
实验步骤:
(1)按图2装配好装置,并检查其气密性;
(2)将相关的试剂放入对应的仪器中;
(3)推动注射器的活塞,把稀盐酸注入锥形瓶内,并固定活塞位置;A中发生的反应方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑;
(4)一段时间后,在a处放置一根带火星的小木条,观察现象.
实验现象:(1)C中干燥管中没有出现蓝色(2)a处带火星的小木条复燃;(3)D处烧杯中水的温度升高.
实验分析:(1)B装置的作用是除去CO2中混有的水蒸气(或干燥);
(2)C装置的作用是检验水蒸气是否除尽;
(3)D装置的烧杯内水温升高的原因是Na2O2和CO2反应要放出(填“吸收”或“放出”)热量.
实验结论:“小木条复燃”说明了Na2O2和CO2反应产生了氧气并放出热量;满足了棉花燃烧的条件.
分析 Ⅰ.实验过程:
二氧化碳灭火的原因:①二氧化碳的密度比空气大;②二氧化碳不能燃烧也不支持燃烧;
Ⅱ.可燃物燃烧的条件是:①与氧气接触;②达到可燃物的着火点;
实验步骤:(1)根据检查气密性的方法解答;
(3)盐酸与碳酸钙反应生成氯化钙和水和二氧化碳;
实验分析:
(1)大多数的固体物质的溶解度随着温度的升高而增大,而氢氧化钙的溶解度却随着温度升高而减小;
(2)浓硫酸具有吸水性,常用来干燥气体,硫酸铜遇水变蓝,常用来检验是否含有水蒸气;
实验结论:
(1)氧气能使带火星的木条复燃;
(2)据石灰水变浑浊可知溶液温度升高,Na2O2和CO2反应放热.
解答 解:实验过程:Ⅰ.
向烧杯中倒入二氧化碳,下面的蜡烛先熄灭,上面的蜡烛后熄灭,说明二氧化碳的密度比空气的密度大;二氧化碳接触火焰,没有燃烧起来,说明不能燃烧;蜡烛熄灭了,说明不能支持燃烧;
Ⅱ、物质燃烧需要三个条件:①物质是可燃物②与氧气接触③温度达到着火点.棉花是可燃物,还需要满足与氧气接触,温度达到着火点;
实验步骤:(3)推动注射器的活塞,把稀盐酸注入锥形瓶内,盐酸与碳酸钙反应生成氯化钙和水和二氧化碳;
实验分析:(1)从图1我们知道,Na2O2和CO2能发生反应,产生氧气,并放出了热量,棉花因有热量使温度达到着火点,就燃烧了起来.在图2中,Na2O2和CO2发生反应,放出热量使石灰水温度升高,氢氧化钙的溶解度减小,析出氢氧化钙固体,从而使澄清石灰水变浑浊;
(2)B装置的作用是除去CO2中混有的水蒸气(或干燥气体),防止水与Na2O2反应生成氧气,造成干扰;C装置的作用是检验水蒸气是否除尽;
故答案为:
Ⅰ.密度比空气大,不可燃烧且不支持燃烧;
Ⅱ.与氧气接触,温度达到着火点;
实验步骤:(3)CaCO3+2HCl═CaCl2+H2O+CO2↑.
实验分析:(1)除去CO2中混有的水蒸气(或干燥);
(2)检验水蒸气是否除尽;
(3)放出.
点评 本题考查内容相对综合,涉及到的知识点有二氧化碳的性质、燃烧的条件、固体物质溶解度影响因素等,主要是运用基础知识去解决新的信息问题,这就要求学生学以致用,综合分析考虑.

| A. | +6 | B. | +4 | C. | +2 | D. | -2 |
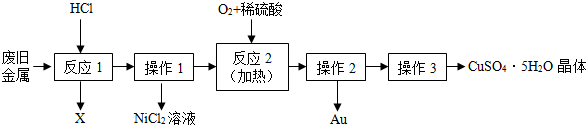
下列说法正确的是( )
| A. | 反应1的生成物为H2O | |
| B. | 操作1和操作2用到玻璃仪器为漏斗、烧杯和玻璃棒 | |
| C. | 三种金属的金属活动性顺序为:Cu>Ni>Au | |
| D. | 反应2的化学方程式为:2Cu+O2+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2CuSO4+2H2O |
| A. | 葡萄酿成美酒 | B. | 白雪缓慢消融 | C. | 霓虹灯光闪烁 | D. | 彩纸折成纸鹤 |
| A. | 木炭+氧气$\stackrel{点燃}{→}$二氧化碳 | B. | 蜡烛+氧气$\stackrel{点燃}{→}$水+二氧化碳 | ||
| C. | 碳酸钙→氧化钙+二氧化碳 | D. | 氨气+氯化氢→氯化铵 |
| A. | CuO+H2SO4═CuSO4+H2O | B. | Cu(OH)2+H2SO4═CuSO4+2H2O | ||
| C. | CO2+2NaOH═Na2CO3+2H2O | D. | CaCO3+2HCl═CaCl2+H2O+CO2↑ |
 .
. 市售塑料袋有的是用聚乙烯[(CH2CH2)n]制成,有的是用聚氯乙烯[(CH2CHCl)n]制成,通过查阅资料可知:(CH2CHCl)n+$\frac{5n}{2}$O2 $\frac{\underline{\;点燃\;}}{\;}$2nCO2+nH2O+nHCl,其中n是上千或上万的数值;HCl气体极易溶于水,有刺鼻气味,其水溶液即是盐酸;鉴别盐酸的方法是加入AgNO3溶液,观察是否产生白色沉淀,二氧化碳与硝酸银溶液不会反应.
市售塑料袋有的是用聚乙烯[(CH2CH2)n]制成,有的是用聚氯乙烯[(CH2CHCl)n]制成,通过查阅资料可知:(CH2CHCl)n+$\frac{5n}{2}$O2 $\frac{\underline{\;点燃\;}}{\;}$2nCO2+nH2O+nHCl,其中n是上千或上万的数值;HCl气体极易溶于水,有刺鼻气味,其水溶液即是盐酸;鉴别盐酸的方法是加入AgNO3溶液,观察是否产生白色沉淀,二氧化碳与硝酸银溶液不会反应.