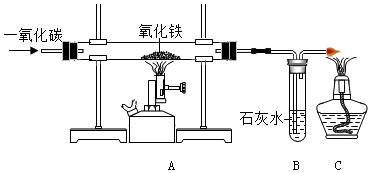
题目内容
1.下表列出了除去物质中少量杂质的方法,其中错误的是( )| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | CO2 | H2O(气) | 将气体通过干燥剂无水氯化钙 |
| B | O2 | CO2 | 将气体通过灼热的铜网 |
| C | Cu | Zn | 加入过量的稀盐酸,过滤,洗涤,干燥 |
| D | FeCl2溶液 | CuCl2 | 加入过量的铁粉,过滤 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、无水氯化钙具有吸水性,且不与二氧化碳反应,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
B、O2能与灼热的铜网反应生成氧化铜,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
C、Zn能与过量的稀盐酸反应生成氯化锌和氢气,铜不与稀盐酸反应,再过滤,洗涤,干燥,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
D、过量的铁粉能与CuCl2溶液反应生成氯化亚铁溶液和铜,再过滤,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
故选:B.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
10.下列物质的用途主要利用其化学性质的是( )
| A. | 干冰用于人工降雨 | B. | 一氧化碳用于炼铁 | ||
| C. | 金刚石用于制玻璃刀 | D. | 氦气用于充探空气球 |
12.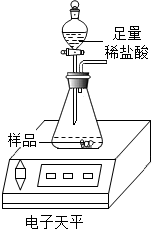 超市卖的纯碱产品中往往会含有少量的氯化钠,化学兴趣小组的同学要通过实验来测定某品牌的纯碱样品中的Na2CO3的质量分数.他们取了纯碱样品11.0g,利用如图装置进行实验测定.数据记录如表:
超市卖的纯碱产品中往往会含有少量的氯化钠,化学兴趣小组的同学要通过实验来测定某品牌的纯碱样品中的Na2CO3的质量分数.他们取了纯碱样品11.0g,利用如图装置进行实验测定.数据记录如表:
计算:
①反应生成CO2的质量为4.4g;
②通过计算确定该品牌纯碱中Na2CO3的质量分数.(写出计算过程,计算结果精确至0.1%.)
③如果测得的结果比实际纯度高,可能的原因是稀盐酸挥发出的HCl气体随CO2气体排出,从而导致所测纯度偏大(答一种即可).
 超市卖的纯碱产品中往往会含有少量的氯化钠,化学兴趣小组的同学要通过实验来测定某品牌的纯碱样品中的Na2CO3的质量分数.他们取了纯碱样品11.0g,利用如图装置进行实验测定.数据记录如表:
超市卖的纯碱产品中往往会含有少量的氯化钠,化学兴趣小组的同学要通过实验来测定某品牌的纯碱样品中的Na2CO3的质量分数.他们取了纯碱样品11.0g,利用如图装置进行实验测定.数据记录如表:| 称量项目 | 称量时间 | 质量/g |
| 样品 | 11.0 | |
| 装置+稀盐酸 | 160.0 | |
| 装置+稀盐酸+样品 | 反应开始后20s | 167.0 |
| 装置+稀盐酸+样品 | 反应开始后30s | 166.6 |
| 装置+稀盐酸+样品 | 反应开始后90s | 166.6 |
①反应生成CO2的质量为4.4g;
②通过计算确定该品牌纯碱中Na2CO3的质量分数.(写出计算过程,计算结果精确至0.1%.)
③如果测得的结果比实际纯度高,可能的原因是稀盐酸挥发出的HCl气体随CO2气体排出,从而导致所测纯度偏大(答一种即可).
8.今年的6月5日是第44各“世界环境日”,也是我国新《环保法》实施后的首个环境日.我国今年的主题是“践行绿色生活”.下列做法不符合这主题的是( )
| A. | 使铁锅代替铝制炊具 | B. | 短途旅行时用自行车代替机动车 | ||
| C. | 合理使用化肥、农药 | D. | 将农田中产生的秸秆就地焚烧 |
 如图是某同学对二氧化碳部分知识构建的网络图(部分反应条件和部分生成物省略).请按下列要求填空:
如图是某同学对二氧化碳部分知识构建的网络图(部分反应条件和部分生成物省略).请按下列要求填空: