题目内容
12.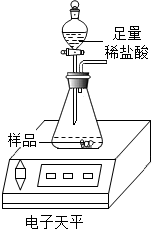 超市卖的纯碱产品中往往会含有少量的氯化钠,化学兴趣小组的同学要通过实验来测定某品牌的纯碱样品中的Na2CO3的质量分数.他们取了纯碱样品11.0g,利用如图装置进行实验测定.数据记录如表:
超市卖的纯碱产品中往往会含有少量的氯化钠,化学兴趣小组的同学要通过实验来测定某品牌的纯碱样品中的Na2CO3的质量分数.他们取了纯碱样品11.0g,利用如图装置进行实验测定.数据记录如表:| 称量项目 | 称量时间 | 质量/g |
| 样品 | 11.0 | |
| 装置+稀盐酸 | 160.0 | |
| 装置+稀盐酸+样品 | 反应开始后20s | 167.0 |
| 装置+稀盐酸+样品 | 反应开始后30s | 166.6 |
| 装置+稀盐酸+样品 | 反应开始后90s | 166.6 |
①反应生成CO2的质量为4.4g;
②通过计算确定该品牌纯碱中Na2CO3的质量分数.(写出计算过程,计算结果精确至0.1%.)
③如果测得的结果比实际纯度高,可能的原因是稀盐酸挥发出的HCl气体随CO2气体排出,从而导致所测纯度偏大(答一种即可).
分析 ①根据质量守恒定律计算反应后生成的二氧化碳的质量;
②根据二氧化碳的质量结合化学方程式计算碳酸钠的质量,再计算质量分数;
③根据盐酸具有挥发性分析回答.
解答 解:①由质量守恒定律可得,减少的质量为逸散到空气中的二氧化碳的质量,则可计算生成二氧化碳的质量为:11.0g+160.0g-166.6g=4.4g.
②设参加反应的碳酸钠的质量为x.
Na2CO3+2HCl=2NaCl+CO2↑+H2O
106 44
x 4.4g
$\frac{106}{44}=\frac{x}{4.4g}$ 则解得 x=10.6g
则食用纯碱中碳酸钠的质量分数为:$\frac{10.6g}{11g}$×100%≈96.4%
③稀盐酸挥发出的HCl气体随CO2气体排出,从而导致所测纯度偏大(或水蒸气随CO2气体排出,从而导致所测纯度偏大).
故答为:(1)4.4;该品牌纯碱中Na2CO3的质量分数为96.4%.(3)稀盐酸挥发出的HCl气体随CO2气体排出,从而导致所测纯度偏大等.
点评 本题主要考查根据化学方程式的计算,难度不大,需要首先搞清反应原理,然后结合题中所给的数据进行解答.

练习册系列答案
相关题目
5.下列关于氧气的说法正确的是( )
| A. | 实验室用分离液态空气法制取氧气 | B. | 氧气能使带火星的木条复燃 | ||
| C. | 灯泡中充入氧气可以延长使用寿命 | D. | 夏天食物腐烂与氧气无关 |
1.下表列出了除去物质中少量杂质的方法,其中错误的是( )
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | CO2 | H2O(气) | 将气体通过干燥剂无水氯化钙 |
| B | O2 | CO2 | 将气体通过灼热的铜网 |
| C | Cu | Zn | 加入过量的稀盐酸,过滤,洗涤,干燥 |
| D | FeCl2溶液 | CuCl2 | 加入过量的铁粉,过滤 |
| A. | A | B. | B | C. | C | D. | D |
17. 构建知识网络是一种重要的学习方法.如图是关于硫酸化学性质的知识网络:“-”表示相连的两种物质能发生反应,“→”表示一种物质能转化为另一种物质,A、B、C分别属于不同类别的化合物.则A、B、C可能是( )
构建知识网络是一种重要的学习方法.如图是关于硫酸化学性质的知识网络:“-”表示相连的两种物质能发生反应,“→”表示一种物质能转化为另一种物质,A、B、C分别属于不同类别的化合物.则A、B、C可能是( )
 构建知识网络是一种重要的学习方法.如图是关于硫酸化学性质的知识网络:“-”表示相连的两种物质能发生反应,“→”表示一种物质能转化为另一种物质,A、B、C分别属于不同类别的化合物.则A、B、C可能是( )
构建知识网络是一种重要的学习方法.如图是关于硫酸化学性质的知识网络:“-”表示相连的两种物质能发生反应,“→”表示一种物质能转化为另一种物质,A、B、C分别属于不同类别的化合物.则A、B、C可能是( )| A. | KOH、CuSO4、Na2CO3 | B. | Ba(OH)2、CuSO4、CuO | ||
| C. | Ca(OH)2、HNO3、K2CO3 | D. | NaOH、HCl、Ba(NO3)2 |
1.下列操作或现象与分子对应的特征不一致的选项是( )
| 选项 | 操作或现象 | 分子的特性 |
| A | 给篮球充气 | 分子间有间隔 |
| B | 100mL酒精和100mL水混合在一起,体积小于200mL | 分子是有质量的 |
| C | 在花园中可闻到花的香味 | 分子是运动的 |
| D | 加热氧化汞可得到金属汞和氧气 | 分子是可以再分的 |
| A. | A | B. | B | C. | C | D. | D |
19. 如图是某化学反应过程的微观示意图,“
如图是某化学反应过程的微观示意图,“ ”“
”“ ”分别代表两种不同的原子.下列说法错误的是( )
”分别代表两种不同的原子.下列说法错误的是( )
 如图是某化学反应过程的微观示意图,“
如图是某化学反应过程的微观示意图,“ ”“
”“ ”分别代表两种不同的原子.下列说法错误的是( )
”分别代表两种不同的原子.下列说法错误的是( )| A. | 该反应属于化合反应 | |
| B. | 分子在化学反应中不可再分 | |
| C. | 甲、乙、丙三种物质都是由分子构成 | |
| D. | 甲、乙、丙的每个分子都是由2个原子构成的 |



