题目内容
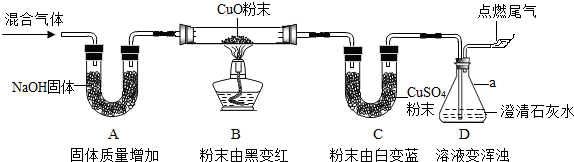
20.某混合气体可能含有CO、H2、CO2、H2O(气)中的一种或几种.为验证其组成,同学们进行实验的装置和现象如下(夹持仪器已省略,假设气体均吸收完全):(1)写出B装置发生的化学方程式H2+CuO$\frac{\underline{\;高温\;}}{\;}$Cu+H2O和CO+CuO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2.
(2)丁认为,由于他们对装置A(填序号)中的实验现象分析不同而导致结论有差异.根据碳酸盐可转化为CO2的性质,丁利用上述实验结束后装置内药品和某种常见试剂进行实验,证明了甲的结论是正确的.请写出丁的实验操作过程与现象将A中固体取出,加入烧杯中,加入过量稀盐酸,无明显现象.
| 结论 | 甲 | 乙 | 丙 |
| 含有CO、H2、H2O(气) | 含有CO、H2、CO2 | 含有CO、H2、CO2、H2O(气) |
分析 由题意可知,按照实验步骤依次进行实验.①氢氧化钠固体具有吸水性和吸收二氧化碳性,氢氧化钠固体质量增加,说明气体中有水蒸气或二氧化碳⇒②灼热的氧化铜,黑色粉末变红色,说明有一氧化碳或氢气或二者的混合气体⇒③无水硫酸铜,白色粉末变蓝,说明上一步反应生成了水,有氢气⇒④澄清的石灰水,石灰水变浑浊,说明②的反应中有二氧化碳气体生成,同时说明混合气体中有CO.
解答 解:(1)CO、H2都具有还原性,能够将黑色的氧化铜还原成红色的铜,反应方程式是CO+CuO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2;H2+CuO$\frac{\underline{\;高温\;}}{\;}$Cu+H2O.
(2)若混合气体中含有CO2、H2O(气),则在A中的氢氧化钠会吸收二氧化碳而成为碳酸钠,所以利用稀盐酸进行验证即可.若加入稀盐酸后,有气泡冒出,则氢氧化钠吸收了二氧化碳气体,若无现象发生,则原混合气体中无二氧化碳气体;
故答案是:(1)H2+CuO$\frac{\underline{\;高温\;}}{\;}$Cu+H2O,CO+CuO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2;
(2)A;将A中固体取出,加入烧杯中,加入过量稀盐酸,无明显现象.
点评 此题主要考查了一氧化碳和氢气还原氧化铜的实验,从反应特点和生成物的性质进行设计,训练同学们的探究能力.

练习册系列答案
相关题目
10.下列现象的描述错误的是( )
| A. | 镁在空气中燃烧发出耀眼的白光 | B. | 铁丝在氧气中燃烧剧烈火星四射 | ||
| C. | 木炭在空气中燃烧发出蓝紫色火焰 | D. | 磷在空气中燃烧产生大量的白雾 |
11.下列实验操作错误的是( )
| A. |  点燃酒精灯 | B. |  读取液体体积 | C. |  倾倒液体 | D. |  给液体试剂加热 |
8.近期中央电视台播出的《舌尖上的中国》很受观众欢迎,该节目主要介绍中国的美食及其制作方法.“饮食健康”是人们普遍的生活追求,下列说法正确是( )
| A. | 用甲醛浸泡海产品 | |
| B. | 在果冻、老酸奶中添加工业明胶 | |
| C. | 在煲好的鸡汤中放入适当的加碘食盐 | |
| D. | 为保持香肠肉质鲜美,添加过量的亚硝酸钠 |
15.5月3日,在德国亥姆霍兹重离子研究中心,欧洲、美国、印度、澳大利亚和日本等多国研究人员在粒子加速器中,用钙离子轰击放射性元素锫,成功生成117号元素.117号元素很快又衰变成115号元素和113号元素.关于113号、115号、117号元素的最本质的区别是( )
| A. | 质子数不同 | B. | 中子数不同 | ||
| C. | 电子数不同 | D. | 相对原子质量不同 |
5.下列变化属于化学变化的是( )
| A. | 食物腐烂 | B. | 酒精挥发 | C. | 瓷碗破碎 | D. | 空气液化 |
12.下列有关实验现象的描述正确的是( )
| A. | 甲烷燃烧生成二氧化碳和水 | B. | 磷在空气中燃烧产生大量白雾 | ||
| C. | 硫在氧气中燃烧产生淡监色火焰 | D. | 镁在空气中燃烧发出耀眼白光 |
9.甲、乙、丙、丁四个化学课外兴趣小组同学分别对各自实验废液中成分进行分析检测,结果如表;检测结果合理的是( )
| 检测小组 | 检测结果 |
| 甲组 | KCl、FeCl3、KOH、HCl |
| 乙组 | NaCl、Ca(NO3)2、K2CO3、HCl |
| 丙组 | NaCl、Mg(NO3)2、K2SO4、H2SO4 |
| 丁组 | KCl、KNO3、K2CO3、KOH |
| A. | 甲组、乙组 | B. | 丙组、丁组 | C. | 甲组、丙组 | D. | 乙组、丁组 |
10. CuSO4是一种重要的化工原料,其有关制备途径如图所示.下列说法不正确的是( )(已知:2Cu+O2+2H2SO4→2CuSO4+2H2O)
CuSO4是一种重要的化工原料,其有关制备途径如图所示.下列说法不正确的是( )(已知:2Cu+O2+2H2SO4→2CuSO4+2H2O)
 CuSO4是一种重要的化工原料,其有关制备途径如图所示.下列说法不正确的是( )(已知:2Cu+O2+2H2SO4→2CuSO4+2H2O)
CuSO4是一种重要的化工原料,其有关制备途径如图所示.下列说法不正确的是( )(已知:2Cu+O2+2H2SO4→2CuSO4+2H2O)| A. | 相对于途径①、③,途径②更好地体现了绿色化学思想 | |
| B. | 途径③中,1mol Cu与足量浓硫酸反应会产生64g SO2气体 | |
| C. | 途径①所用混酸中H2SO4与HNO3物质的量之比最好为3:2 | |
| D. | 1mol Cu分别按照途径②、③中,被还原的H2SO4的质量之比为1:1 |