题目内容
12.下列有关实验现象的描述正确的是( )| A. | 甲烷燃烧生成二氧化碳和水 | B. | 磷在空气中燃烧产生大量白雾 | ||
| C. | 硫在氧气中燃烧产生淡监色火焰 | D. | 镁在空气中燃烧发出耀眼白光 |
分析 A、根据甲烷燃烧的现象进行分析判断.
B、根据磷在空气中燃烧的现象进行分析判断.
C、根据硫在氧气中燃烧的现象进行分析判断.
D、根据镁条燃烧的现象进行分析判断.
解答 解:A、甲烷燃烧生成二氧化碳和水属于结论,不是现象,故选项说法错误.
B、红磷在空气中燃烧,产生大量的白烟,而不是白雾,故选项说法错误.
C、硫在氧气中燃烧,发出明亮的蓝紫色火焰,故选项说法错误.
D、镁条空气中燃烧,发出耀眼的白光,生成白色固体,故选项说法正确.
故选:D.
点评 本题难度不大,掌握常见物质燃烧的现象即可正确解答,在描述物质燃烧的现象时,需要注意光和火焰、烟和雾的区别.

练习册系列答案
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案
相关题目
2.某兴趣小组为探究铝镁合金的组成,取16g铝镁合金样品,将60g氢氧化钠溶液平均分成三份分三次次加入到样品中(镁与氢氧化钠溶液不反应,铝与氢氧化钠溶液反应的化学方程式为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑,充分反应后,过滤出固体,将其洗涤、干燥、称量,得实验数据如下:
试计算:
(1)分析表中数据可知,第二次反应结束后,剩余固体质量m是5.2克.
(2)该合金中,镁元素的质量为4克.
(3)所用氢氧化钠溶液中溶质的质量分数.
| 所加氢氧化钠溶液的次数 | 第一次 | 第二次 | 第三次 |
| 剩余固体的质量/g | 10.6 | m | 4.0 |
(1)分析表中数据可知,第二次反应结束后,剩余固体质量m是5.2克.
(2)该合金中,镁元素的质量为4克.
(3)所用氢氧化钠溶液中溶质的质量分数.
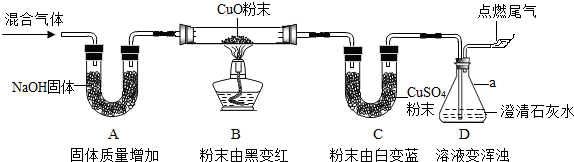
20.某混合气体可能含有CO、H2、CO2、H2O(气)中的一种或几种.为验证其组成,同学们进行实验的装置和现象如下(夹持仪器已省略,假设气体均吸收完全):
(1)写出B装置发生的化学方程式H2+CuO$\frac{\underline{\;高温\;}}{\;}$Cu+H2O和CO+CuO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2.
(2)丁认为,由于他们对装置A(填序号)中的实验现象分析不同而导致结论有差异.根据碳酸盐可转化为CO2的性质,丁利用上述实验结束后装置内药品和某种常见试剂进行实验,证明了甲的结论是正确的.请写出丁的实验操作过程与现象将A中固体取出,加入烧杯中,加入过量稀盐酸,无明显现象.
(1)写出B装置发生的化学方程式H2+CuO$\frac{\underline{\;高温\;}}{\;}$Cu+H2O和CO+CuO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2.
(2)丁认为,由于他们对装置A(填序号)中的实验现象分析不同而导致结论有差异.根据碳酸盐可转化为CO2的性质,丁利用上述实验结束后装置内药品和某种常见试剂进行实验,证明了甲的结论是正确的.请写出丁的实验操作过程与现象将A中固体取出,加入烧杯中,加入过量稀盐酸,无明显现象.

| 结论 | 甲 | 乙 | 丙 |
| 含有CO、H2、H2O(气) | 含有CO、H2、CO2 | 含有CO、H2、CO2、H2O(气) |
7.某人患有甲状腺肿大症,他所缺乏的元素主要是( )
| A. | 钙元素 | B. | 锌元素 | C. | 碘元素 | D. | 铁元素 |
1.在一密闭容器内有A、B、C、D四种物质,在一定条件下发生化学反应,一段时间后,测得反应前后各物质的质量如表,则下列说法中正确的是( )
| 物 质 | A | B | C | D |
| 反应前物质质量(g) | 10 | 90 | 8 | 2 |
| 反应后物质质量(g) | 38 | 56 | 14 | X |
| A. | 该反应中D一定是催化剂 | B. | 根据质量守恒定律,X的值为0 | ||
| C. | 该反应是分解反应 | D. | 该反应是复分解反应 |
2.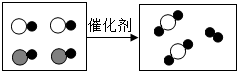 在催化剂的作用下,尾气转换器可将汽车中的有毒气体转换成无毒气体,其微观过程如图所示(不同圆球代表不同原子).下列说法正确的是( )
在催化剂的作用下,尾气转换器可将汽车中的有毒气体转换成无毒气体,其微观过程如图所示(不同圆球代表不同原子).下列说法正确的是( )
 在催化剂的作用下,尾气转换器可将汽车中的有毒气体转换成无毒气体,其微观过程如图所示(不同圆球代表不同原子).下列说法正确的是( )
在催化剂的作用下,尾气转换器可将汽车中的有毒气体转换成无毒气体,其微观过程如图所示(不同圆球代表不同原子).下列说法正确的是( )| A. | 生成物全部是化合物 | B. | 参加反应的两种分子个数比为3:2 | ||
| C. | 反应后分子个数变少了 | D. | 反应后原子个数变少了 |
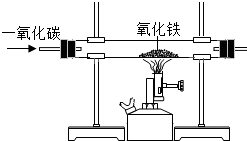 某同学设计了用一氧化碳与氧化铁反应来探究炼铁原理的装置,如图.
某同学设计了用一氧化碳与氧化铁反应来探究炼铁原理的装置,如图.