题目内容
16.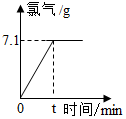 氯化钠是一种重要的化工原料,电解氯化钠溶液可制得氯气、氢氧化钠等物质,发生的化学反应如下:2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$ Cl2↑+H2↑+2NaOH 现取一定质量的溶质质量分数为10%的氯化钠溶液进行电解,当氯化钠完全反应时,停止通电.生成氯气的质量与反应时间的关系如图所示.请计算:
氯化钠是一种重要的化工原料,电解氯化钠溶液可制得氯气、氢氧化钠等物质,发生的化学反应如下:2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$ Cl2↑+H2↑+2NaOH 现取一定质量的溶质质量分数为10%的氯化钠溶液进行电解,当氯化钠完全反应时,停止通电.生成氯气的质量与反应时间的关系如图所示.请计算:(1)生成氢气多少克?
(2)参加反应的10%的氯化钠溶液需多少克?
分析 根据反应的化学方程式及其提供的数据可以进行相关方面的计算和判断.
解答 解:(1)设氯化钠质量为x,生成氢气质量为y
2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$Cl2↑+H2↑+2NaOH,
117 71 2
x 7.1g y
$\frac{117}{x}=\frac{71}{7.1g}=\frac{2}{y}$
x=11.7g,y=0.2g
(2)参加反应的10%的氯化钠溶液质量为:11.7g÷10%=117g,
答:(1)反应生成H2的质量是0.2g. (2)参加反应的10%的氯化钠溶液质量为117g.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
6.一包氯化镁和氯化钠组成的混合物中,小亮同学称取该混合物样品23.7g,完全溶于水中,然后取用一定溶质质量分数的氢氧化钠溶液100g,平均分四次加入其中,充分振荡后,测得实验数据如下表所示,请分析并进行相关的计算:
(1)上表中X的数值是5.8;
(2)原固体混合物样品中氯化镁的质量;
(3)恰好完全反应时,所得溶液的溶质质量分数是多少?
| 次数 | 1 | 2 | 3 | 4 |
| 加入氢氧化钠溶液的质量(g) | 25 | 25 | 25 | 25 |
| 生成沉淀的质量(g) | 2.9 | X | 8.7 | 8.7 |
(2)原固体混合物样品中氯化镁的质量;
(3)恰好完全反应时,所得溶液的溶质质量分数是多少?
7.下列各组物质中,都由原子构成的一组是( )
| A. | 氧气和硫酸铜 | B. | 水和氨气 | C. | 汞和氯化钠 | D. | 金和金刚石 |
11.要完成下列变化,能用盐酸经过一步反应实现的是( )
(1)CaO---CaCl2 (2)Fe2O3---FeCl2(3)Cu---CuCl2 (4)Fe---F eCl3.
(1)CaO---CaCl2 (2)Fe2O3---FeCl2(3)Cu---CuCl2 (4)Fe---F eCl3.
| A. | 只有(1) | B. | 只有(2) | C. | (1)(4) | D. | (1)(3)(4) |
1.下列说法正确的是( )
①氧化物中的氧被夺去的反应叫还原反应.
②分子是化学变化中的最小微粒.
③具有相同核电荷数的物质总称为元素.
④混合物一定由2种或2种以上的元素组成.
⑤电离时生成的阴离子中有氢氧根离子的化合物就是碱.
⑥若温度不变,向饱和Ca(OH)2溶液中加入生石灰,不能增大溶液的质量分数.
①氧化物中的氧被夺去的反应叫还原反应.
②分子是化学变化中的最小微粒.
③具有相同核电荷数的物质总称为元素.
④混合物一定由2种或2种以上的元素组成.
⑤电离时生成的阴离子中有氢氧根离子的化合物就是碱.
⑥若温度不变,向饱和Ca(OH)2溶液中加入生石灰,不能增大溶液的质量分数.
| A. | ①③⑥ | B. | ②④⑤ | C. | ①⑥ | D. | 只有④ |
8.2010年上海世博会中国馆-“东方之冠”给人强烈的视觉冲击,其底部为四根巨型钢筋混凝土核心筒.其中钢属于( )
| A. | 金属材料 | B. | 合成材料 | C. | 天然材料 | D. | 复合材料 |
6.下列物质与澄清石灰水反应不能产生沉淀的是( )
| A. |  | B. |  | C. | 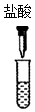 | D. | 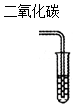 |



