题目内容
1.下列说法正确的是( )①氧化物中的氧被夺去的反应叫还原反应.
②分子是化学变化中的最小微粒.
③具有相同核电荷数的物质总称为元素.
④混合物一定由2种或2种以上的元素组成.
⑤电离时生成的阴离子中有氢氧根离子的化合物就是碱.
⑥若温度不变,向饱和Ca(OH)2溶液中加入生石灰,不能增大溶液的质量分数.
| A. | ①③⑥ | B. | ②④⑤ | C. | ①⑥ | D. | 只有④ |
分析 ①根据还原反应的定义分析;
②根据化学反应的实质解答;
③根据元素的定义解答;
④根据混合物的定义解答;
⑤根据碱是指电离时电离出的阴离子全部是氢氧根离子的化合物解答;
⑥根据在同一温度下,氢氧化钙的饱和溶液的溶质质量分数不变解答.
解答 解:
①氧化物里的氧被夺去的反应叫还原反应,故正确;
②在化学反应中,分子可以再分,原子不能再分,原子是化学变化中的最小微粒,故错误;
③元素是具有相同核电荷数(即核内质子数)的一类原子的总称,故错误;
④混合物一定由2种或2种以上的物质组成,不是元素,故错误;
⑤电离时生成的阴离子都是氢氧根离子的化合物是碱,故错误;
⑥氧化钙能与水反应生成氢氧化钙,消耗水,故溶液的质量减小,在同一温度下,氢氧化钙的饱和溶液的溶质质量分数不变,故正确.
答案:C
点评 本题考查类推法的应用,学生应能根据不同知识的特点类推,不能盲目类推,并注意知识点与方法的有机结合,做到具体问题能具体分析.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
11.如图是甲、乙两种固体物质的溶解度曲线,下列有关叙述正确的是( )


| A. | 0℃时.甲物质的溶解度为20 | |
| B. | 10℃时.甲.乙两种物质的溶解度相等 | |
| C. | 30℃时.甲物质饱和溶液的质量分数为60% | |
| D. | 除去甲物质中少量乙物质可采取蒸发结晶的方法 |
12.下列化学方程式中符合题意且书写正确的是( )
| A. | 正常雨水呈弱酸性原因:CO2+H2O=H2CO3 | |
| B. | 用稀盐酸除去铁表面铁锈:FeO+2HCI=FeCl2+2H2O | |
| C. | 生活中用天然气作燃料:C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O | |
| D. | 工业上用熟石灰制烧碱:Ca(OH)2+2NaNO3=Ca(NO3)2+2NaOH |
9.化学用语是国际通用的化学语言,下列有关说法正确的是( )
| A. | 2O表示两个氧分子 | B. | 钠离子的符号为Na+ | ||
| C. | 氯化铁的化学式FeCl2 | D. | H2O中含有氧分子 |
6.下列现象与物质状态变化的联系正确的是( )
| A. | 冬天从嘴里呼出的“白汽”:汽化 | |
| B. | 电流过大时,电路中保险丝熔断:熔化 | |
| C. | 湿衣服凉干:液化 | |
| D. | 硫酸铜溶液中加入氢氧化钠溶液产生蓝色沉淀:凝固 |
13.下列所示的实验操作正确的是( )
| A. |  点燃酒精灯 | B. |  称量物体质量 | ||
| C. |  读取液体体积 | D. |  调粗准焦螺旋使镜筒下降 |
10.2016年秋季开学,合肥市在全省率先推出“午餐工程”,在下列午餐食谱中蛋白质含量最丰富的是( )
| A. |  苹果 苹果 | B. |  红烧排骨 红烧排骨 | C. |  猕猴桃 猕猴桃 | D. |  面条 面条 |
11.某样品为铜和氧化铁的混合物.王伟同学为测定该样品中金属铜的含量,进行了如下实验:取用10克此样品,将某硫酸溶液分三次加入使之充分反应.每次所用硫酸的质量与反应后剩余固体质量见下表.
求:(1)此样品中金属铜和氧化铁的质量比为1:9.
(2)所用硫酸溶液的溶质质量分数.
| 次 | 加入硫酸的质量/克 | 剩余固体的质量/克 |
| 1 | 15 | 6 |
| 2 | 15 | 2 |
| 3 | 15 | 1 |
(2)所用硫酸溶液的溶质质量分数.
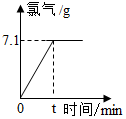 氯化钠是一种重要的化工原料,电解氯化钠溶液可制得氯气、氢氧化钠等物质,发生的化学反应如下:2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$ Cl2↑+H2↑+2NaOH 现取一定质量的溶质质量分数为10%的氯化钠溶液进行电解,当氯化钠完全反应时,停止通电.生成氯气的质量与反应时间的关系如图所示.请计算:
氯化钠是一种重要的化工原料,电解氯化钠溶液可制得氯气、氢氧化钠等物质,发生的化学反应如下:2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$ Cl2↑+H2↑+2NaOH 现取一定质量的溶质质量分数为10%的氯化钠溶液进行电解,当氯化钠完全反应时,停止通电.生成氯气的质量与反应时间的关系如图所示.请计算: