题目内容
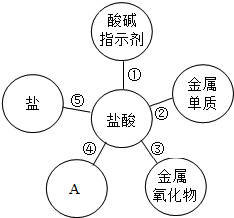 归纳是学习的重要方法,小红在复习盐酸的性质时,归纳出盐酸的五条化学性质(如图所示,连线表示相互反应).
归纳是学习的重要方法,小红在复习盐酸的性质时,归纳出盐酸的五条化学性质(如图所示,连线表示相互反应).(1)为了验证性质①,小红将紫色石蕊溶液滴加到盐酸溶液中,溶液变
(2)图中A所代表的物质类别是
(3)盐酸的性质③决定了盐酸可用于清除铁锈(主要成分是Fe2O3),该反应的化学方程式是
(4)镁和锌可以用来验证盐酸的性质②,小红要探究镁和锌与盐酸反应的快慢,需要控制不变(相同)的量是
A.两种金属的形状B.盐酸的质量分数 C.反应容器的大小D.温度.
考点:酸的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见的酸 酸的通性
分析:(1)利用石蕊遇酸的变色情况分析即可.
(2)根据酸的化学性质:能与活泼金属、金属氧化物、酸碱指示剂、盐、碱等反应,进行分析解答.
(3)铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,写出反应的化学方程式即可.
(4)控制变量法要创设相同的外部条件,分析对镁和锌与盐酸反应的快慢可能有影响的因素.
(2)根据酸的化学性质:能与活泼金属、金属氧化物、酸碱指示剂、盐、碱等反应,进行分析解答.
(3)铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,写出反应的化学方程式即可.
(4)控制变量法要创设相同的外部条件,分析对镁和锌与盐酸反应的快慢可能有影响的因素.
解答:解:(1)石蕊遇酸性溶液会变红色,所以将紫色石蕊试液滴加到盐酸溶液中溶液变红.
(2)盐酸除了能与酸碱指示剂、金属氧化物、金属、盐反应外,还能与碱发生中和反应,故A的类别是碱.
(3)铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O.
(4)控制变量法要创设相同的外部条件,探究镁和锌与盐酸反应的快慢,需要控制不变的条件就是对反应速度可能有影响的因素,分析可知四个因素中只有容器的大小对反应速度无影响.
故答案为:(4分)(1)红(2)碱(3)6HCl+Fe2O3═2FeCl3+3H2O (4)ABD
(2)盐酸除了能与酸碱指示剂、金属氧化物、金属、盐反应外,还能与碱发生中和反应,故A的类别是碱.
(3)铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O.
(4)控制变量法要创设相同的外部条件,探究镁和锌与盐酸反应的快慢,需要控制不变的条件就是对反应速度可能有影响的因素,分析可知四个因素中只有容器的大小对反应速度无影响.
故答案为:(4分)(1)红(2)碱(3)6HCl+Fe2O3═2FeCl3+3H2O (4)ABD
点评:本题难度不大,熟练掌握酸的化学性质、化学方程式的书写等并能灵活运用是正确解答本题的关键.

练习册系列答案
相关题目
如图所示的实验操作中正确的是( )
A、 |
B、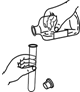 |
C、 |
D、 |
甲基咪唑是一种微黄色的固体,化学式为C4H6N2,下列关于它的说法正确的是( )
| A、该物质中碳、氢、氮三种元素的质量比为4:6:2 |
| B、该物质是由4个碳原子、6个氢原子、2个氮原子构成 |
| C、该物质是由分子构成,每个分子由碳、氢、氮三种元素组成 |
| D、该物质中碳元素的质量分数约为58.5% |
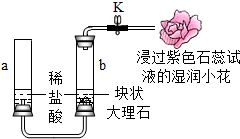 某实验小组用如图装置研究CO2的性质.提示:
某实验小组用如图装置研究CO2的性质.提示: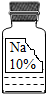 实验室有一瓶保存不当的试剂(如图所示),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.
实验室有一瓶保存不当的试剂(如图所示),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.