题目内容
15.在硫酸铜和硫酸锌的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤出的固体中滴加稀硫酸,没有气泡产生,则滤出的固体是Cu(填化学式,下同),滤液中一定含有的溶质为ZnSO4、FeSO4,有关反应方程式为Fe+CuSO4═FeSO4+Cu.分析 锌比铁活泼,铁比铜活泼,在硫酸铜和硫酸锌的混合溶液中加入一定量的铁粉时,铁能和硫酸铜反应生成硫酸亚铁和铜.
解答 解:向滤出的固体中滴加稀硫酸,没有气泡产生,说明铁已经完全反应,则滤出的固体是Cu,滤液中一定含有的溶质是没有反应的ZnSO4和反应生成的FeSO4,铁能和硫酸铜反应生成硫酸亚铁和铜,反应方程式为:Fe+CuSO4═FeSO4+Cu.
故填:Cu;ZnSO4;FeSO4;Fe+CuSO4═FeSO4+Cu.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案
相关题目
6.要配制50g质量分数为20%的硝酸钾溶液,现提供25g质量分数为40%的硝酸钾溶液、20g质量分数为15%的硝酸钾溶液及足够多的固体硝酸钾和水,请选用上述药品,设计三套配制方案填入如表.
| 配制方案(只说明配制时所需各种药品药量) | |
| 方案一 | |
| 方案二 | |
| 方案三 |
10.将无色酚酞试液滴入下列溶液中,都变红色的是( )
| A. | 食醋、石灰水 | B. | 石灰水、盐酸 | ||
| C. | 石灰水、氢氧化钠溶液 | D. | 食醋、盐酸 |
4.某同学对气体的实验室制法作了以下探究,请根据图1回答下列问题:
(1)写出标有序号的仪器的名称.

a分液漏斗;b水槽.
〔2〕如果要在实验室制取二氧化碳,则应该选择的装置组合为AD(填字母),不能用C装置收集气体的理由是:二氧化碳能溶于水(请用文字说明).
〔3〕若某兴趣小组同学用以上某装置对实验室制备氧气的条件进行如下探究实验.
①为探究催化剂的种类对氯酸钾分解速度的影响,甲同学设计以下对比实验:
Ⅰ.将3.0g KClO3与1.0g MnO2均匀混合加热
Ⅱ.将x g KClO3与1.0g CuO均匀混合加热
在相同温度下,比较两组实验产生O2的快慢.
Ⅰ中反应的化学方程式是2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;Ⅱ中x的值应为3.0.
②乙同学探究了影响双氧水分解速度的某种因素.实验数据记录如下:
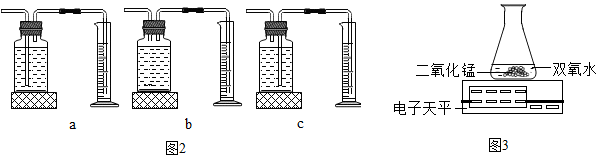
本实验中,测量O2体积的装置是c(填图2编号).实验结论:在相同条件下,双氧水中溶质的质量分数越 大(填“大”或“小”),双氧水分解得越快.
丙同学用图3装置进行实验也能达到实验目的,其还需要的实验仪器是②(填编号)
①温度计 ②计时器 ③密度计 ④刻度尺.
(1)写出标有序号的仪器的名称.

a分液漏斗;b水槽.
〔2〕如果要在实验室制取二氧化碳,则应该选择的装置组合为AD(填字母),不能用C装置收集气体的理由是:二氧化碳能溶于水(请用文字说明).
〔3〕若某兴趣小组同学用以上某装置对实验室制备氧气的条件进行如下探究实验.
①为探究催化剂的种类对氯酸钾分解速度的影响,甲同学设计以下对比实验:
Ⅰ.将3.0g KClO3与1.0g MnO2均匀混合加热
Ⅱ.将x g KClO3与1.0g CuO均匀混合加热
在相同温度下,比较两组实验产生O2的快慢.
Ⅰ中反应的化学方程式是2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;Ⅱ中x的值应为3.0.
②乙同学探究了影响双氧水分解速度的某种因素.实验数据记录如下:
| 双氧水的质量 | 双氧水中溶质的质量分数 | MnO2的质量 | 相同时间内产生O2体积 | |
| Ⅰ | 50.0g | 1% | 0.1g | 9mL |
| Ⅱ | 50.0g | 2% | 0.1g | 16mL |
| Ⅲ | 50.0g | 4% | 0.1g | 31mL |

本实验中,测量O2体积的装置是c(填图2编号).实验结论:在相同条件下,双氧水中溶质的质量分数越 大(填“大”或“小”),双氧水分解得越快.
丙同学用图3装置进行实验也能达到实验目的,其还需要的实验仪器是②(填编号)
①温度计 ②计时器 ③密度计 ④刻度尺.
