题目内容
4.将一定质量的铜锌合金的粉末加入到一定量的硝酸银溶液中充分反应后过滤,向滤渣中滴加少量的稀盐酸,有气泡产生,下列说法正确的是( )| A. | 滤液中的溶质一定含有硝酸铜 | B. | 滤液中溶质一定不含硝酸银 | ||
| C. | 滤渣中可能含有银和锌 | D. | 滤渣中一定没有铜 |
分析 根据金属活动性强弱关系:锌>氢>铜>银,将铜锌合金的粉末加入到硝酸银溶液中,锌先与硝酸银发生反应,待锌完全反应后,铜再与硝酸银发生反应,所以锌的量会对反应结果产生很大影响,向充分反应后所得滤渣中滴加少量的稀盐酸,有气泡产生,说明反应后剩余固体中含有锌,铜还没有反应进行分析.
解答 解:由金属活动性强弱关系:锌>氢>铜>银可知,将铜锌合金的粉末加入到硝酸银溶液中,锌先与硝酸银发生反应,待锌完全反应后,铜再与硝酸银发生反应,所以锌的量会对反应结果产生很大影响,向充分反应后所得滤渣中滴加少量的稀盐酸,有气泡产生,说明反应后剩余固体中含有锌,铜还没有反应,所以
A、铜没有参与反应,所以滤液中的溶质一定不含有硝酸铜,故A错误;
B、锌有剩余,所以滤液中溶质一定不含硝酸银,故B正确;
C、滤渣中一定含有铜、银和锌,故C错误;
D、滤渣中一定有铜,故D错误.
故选:B.
点评 将活动性强的金属混合物放入活动性弱的金属的盐溶液中,金属由强到弱依次与盐发生反应,即金属混合物中活动性最弱的金属首先与盐溶液发生反应,依此类推.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
3.某纯净物3g在氧气中完全燃烧,生成8.8g二氧化碳和5.4g水.下列说法不正确的是( )
| A. | 该纯净物中含有C、H元素,不含O元素 | |
| B. | 该反应中O2和CO2的质量比为14:11 | |
| C. | 该反应中O2和H2O的分子数之比为7:6 | |
| D. | 该纯净物中C、H原子的个数比为1:4 |
16.食品保鲜的措施有添加防腐剂、充填气体、放置干燥剂和脱氧剂等.
请从A或B两题中任选1个作答,若两题均作答,按A计分.
请从A或B两题中任选1个作答,若两题均作答,按A计分.
| A | B |
| 丙酸钠是一种常用的防腐剂,其化学式为C3H5O2Na.碳元素和氧元素的质量比为9:8. | 山梨酸钾(C6H7KO2)是国际粮农组织和卫生组织推荐的高效安全的防腐保鲜剂. 山梨酸钾中钾质量分数为26%,其计算式为$\frac{39}{12×6+1×7+39+16×2}×100%$. |
14.浓硫酸和浓盐酸敞口放置在空气中一段时间后,溶液中( )
| A. | 溶液的质量都增大 | |
| B. | 溶质的质量分数都变小 | |
| C. | 溶质的质量分数前者变大,后者变小 | |
| D. | 溶质的质量分数都变大 |
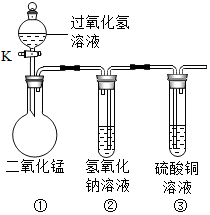 在“创新实验装置”的竞赛中,某化学兴趣小组的同学设计了如图所示的装置.
在“创新实验装置”的竞赛中,某化学兴趣小组的同学设计了如图所示的装置.