题目内容
3.某纯净物3g在氧气中完全燃烧,生成8.8g二氧化碳和5.4g水.下列说法不正确的是( )| A. | 该纯净物中含有C、H元素,不含O元素 | |
| B. | 该反应中O2和CO2的质量比为14:11 | |
| C. | 该反应中O2和H2O的分子数之比为7:6 | |
| D. | 该纯净物中C、H原子的个数比为1:4 |
分析 根据质量守恒定律的含义(即六不变)中的“元素的种类不变”可知,生成物所含的碳、氢、氧三种元素中的碳元素和氢元素一定来自于纯净物,至于氧元素可能全部来自于氧气,也可能部分来自于氧气,另一部分则来自于3g物质,可根据元素的质量不变进行判断;根据生成物CO2和H2O中C、H元素质量,让碳氢元素的质量分别除以各自的相对原子质量再相比,就可以得到该物质中碳氢两元素的原子个数比.
解答 解:A、根据质量守恒定律可知,化学反应前后元素的种类保持不变;说明该物质一定含有氢元素和碳元素,可能含有氧元素;
又因为:二氧化碳中碳元素的质量等于8.8g×$\frac{12}{44}$=2.4g,水中氢元素的质量等于5.4g×$\frac{2}{18}$=0.6g,
因此氢元素和碳元素的质量之和是2.4g+0.6g═3.0g,说明该物质仅含有碳元素和氢元素,故说法正确.
B、根据质量守恒定律可知,参加反应的氧气的质量为8.8g+5.4g-3g=11.2g,则该反应中O2和CO2的质量比为11.2g:8.8g=14:11,故说法正确;
C、反应中O2和H2O的分子数之比为$\frac{11.2g}{32}$:$\frac{5.4g}{18}$=7:6,故说法正确;
D、该纯净物中C、H原子的个数比为$\frac{2.4g}{12}$:$\frac{0.6g}{1}$=1:3,故错误.
故选:D.
点评 本题主要考查有关化学式的计算,难度稍大.关键是找到确定该物质的元素组成、元素质量和原子个数比的方法.

练习册系列答案
 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案
相关题目
14.某化工厂按如下步骤进行生产:(1)以煤为燃料煅烧石灰石;(2)用饱和碳酸钠溶液充分吸收(1)中产生的二氧化碳(Na2CO3+CO2+H2O═2NaHCO3);(3)使步骤(1)中产生的氧化钙跟水反应;(4)熟石灰与碳酸钠溶液反应.该厂生产过程中所涉及的物质有①石灰石;②碳酸钠;③碳酸氢钠;④烧碱;⑤二氧化碳;⑥熟石灰.下列说法正确的是( )
| A. | 起始原料是①③ | B. | 起始原料是②⑥ | C. | 最终产品是⑤⑥ | D. | 最终产品是③④ |
11.2017年5月9曰,我国发布了四种人造新元素的中文名称,其中115号镆元素 的“镆”取自古代剑名“镆铘”,下列说法不正确的是( )
| A. | 镆属于金属元素 | B. | 镆铘剑含有镆元素 | ||
| C. | 镆原子的质子数为115 | D. | 镆铘剑由合金铸造 |
15.下列变化属于化学变化的是( )
| A. | 干冰升华 | B. | 白磷燃烧 | C. | 铁丝折弯 | D. | 酒精挥发 |
3.下列物质加入水中能形成无色溶液的是( )
| A. | 面粉 | B. | 硫酸铜 | C. | 氯化钠 | D. | 冰 |
4.将一定质量的铜锌合金的粉末加入到一定量的硝酸银溶液中充分反应后过滤,向滤渣中滴加少量的稀盐酸,有气泡产生,下列说法正确的是( )
| A. | 滤液中的溶质一定含有硝酸铜 | B. | 滤液中溶质一定不含硝酸银 | ||
| C. | 滤渣中可能含有银和锌 | D. | 滤渣中一定没有铜 |
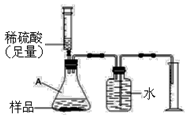 侯德榜是我国著名的化学家.由他发明的侯氏制碱法制得的纯碱中含有少量氯化钠杂质.某化学兴趣小组的同学为了测定该厂生产的纯碱是否属于优等品(国家规定:优等品中碳酸钠的质量分数不低于99.2%),设计了如下两种实验方案
侯德榜是我国著名的化学家.由他发明的侯氏制碱法制得的纯碱中含有少量氯化钠杂质.某化学兴趣小组的同学为了测定该厂生产的纯碱是否属于优等品(国家规定:优等品中碳酸钠的质量分数不低于99.2%),设计了如下两种实验方案
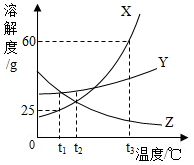 如图所示为X、Y、Z三种固体物质(不含结晶水)的溶解度曲线,请回答下列问题:
如图所示为X、Y、Z三种固体物质(不含结晶水)的溶解度曲线,请回答下列问题: