题目内容
8.镁合金的强度高、机械性能好.这些特性使金属镁成为制造汽车、飞机、火箭的重要材料,从而获得“国防金属”的美誉.海水提镁是国际上的主要趋势,工业流程图如图1;
其步骤为:
I.将海边大量存在的贝壳(主要成分为CaCO3)煅烧成生石灰,并将生石灰制成石灰乳
Ⅱ.将石灰乳加入到海水反应池中,经过沉降、过滤得到Mg(OH)2沉淀
Ⅲ.在Mg(OH)2沉淀中加入盐酸中和得到MgCl2溶液,再经蒸发结晶得到MgCl2•6H2O
Ⅳ.将MgCl2•6H2O在一定条件下加热得到无水MgCl2
V.电解熔融的无水MgCl2可得到Mg
(1)请根据上述步骤回答问题:
①写出步骤I、Ⅲ的有关化学方程式:--
I.贝壳煅烧成生石灰CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
Ⅲ.Mg(OH)2沉淀中加入盐酸中和Mg(OH)2+2HCl=MgCl2+2H2O
②步骤I~V中有分解反应的是(填写步骤序号):I、Ⅳ、V.
③步骤Ⅲ中的蒸发是利用风吹日晒来完成的,而在实验室中进行蒸发操作需要的主要仪器有蒸发皿、玻璃棒、酒精灯、带铁圈的铁架台、坩埚钳等.
④上述海水提镁的流程中,采取了哪些措施来降低成本、减少污染的?请写出其中一点:电解产生的氯气用于生产HCl.
(2)回答下列问题;
①如图2元素的某种粒子结构示意图,该图表示(填序号)C.
A.分子 B.原于 C.阳离子 D.阴离子
②镁原子在化学反应中容易失去电子,镁是一种(填“活泼”或“不活泼”)活泼金属,
除了能与氧气反应,还可以与氮气,二氧化碳等反应.
(3)为测定约含镁30%的镁铝合金(不含其它元素)中 镁的质量分数.
①第一小组设计下列实验方案:称量as镁铝合金粉末,放在如图3装置的惰性电热板上,通电使其充分灼烧.
讨论一:欲计算镁的质量分数,该实验中还需测定的一种数据是完全反应后生成的固体的质量.
讨论二:若用空气代替O2进行实验,对测定结果(填“有”或“无’)有影响.
②第二小组没计下列实验方案:称取bg镁铝合金,与足量的稀盐酸完全反应.
欲计算镁的质量分数,该实验中还需测定的一种数据是充分反应后生成的氢气的质量(体积).
分析 (1)①根据化学方程式的书写方法来分析;②根据分解反应的概念分析即可;③根据蒸发操作所用到的仪器分析即可;④根据工艺流程图来分析.
(2)根据微粒结构示意图来分析;
(3)①已知镁铝合金为a克,镁铝合金燃烧后生成氧化镁与氧化铝,称出反应后固体的质量为b克,我们就可以设镁铝合金中镁的质量为x,则铝的质量为(a-x)g;设生成固体中氧化镁的质量为y,则氧化铝的质量为(b-y)g;然后根据化学方程式列出比例式,解方程组求解即可.
②已知镁铝合金为a克,镁铝合金与酸后会生成氢气,称出反应后生成氢气的质量为c克,我们就可以设镁铝合金中镁的质量为m,则铝的质量为(a-m)g;设镁与酸反应生成氢气的质量为n,则铝与酸反应生成氢气的质量为(c-n)g;然后根据化学方程式列出比例式,解方程组求解即可.
解答 解:(1):①贝壳的主要成分是碳酸钙,锻烧碳酸钙生成氧化钙和二氧化碳,反应的原理是:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;氧化钙与水反应生成氢氧化钙;向Mg(OH)2沉淀中加入盐酸所发生的反应是:Mg(OH)2+2HCl=MgCl2+2H2O,故填:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;Mg(OH)2+2HCl=MgCl2+2H2O;
②分解反应的概念:由一种物质生成两种或两种以上的物质的反应,I、Ⅳ、V所涉及到的方程式分别为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑; MgCl2•6H2O$\frac{\underline{\;\;△\;\;}}{\;}$MgCl2+6H2O; MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑;故答案为:I、Ⅳ、V;
③蒸发过程所用到的仪器有蒸发皿、玻璃棒、酒精灯、带铁圈的铁架台、坩埚钳等,故答案为:蒸发皿;玻璃棒;
④电解产生的Cl2用于制取HCl气体,实现盐酸循环利用,减少了环境污染.故填:电解产生的氯气用于生产HCl.
(2)①该粒子核内有12个质子,核外有10个电子,是带两个单位正电荷的镁离子,属于阳离子;故填:C;
②镁是一种化学性质活泼的金属;故填:活泼;
(3)①欲计算镁的质量分数,该实验中还需测定的一种数据是:完全反应后生成的固体的质量.故填:完全反应后生成的固体的质量.
②因为镁除了能与氧气反应,还可以与氮气,二氧化碳等反应.故填:有.
③欲计算镁的质量分数,该实验中还需测定的一种数据是:充分反应后生成的氢气的质量.故填:充分反应后生成的氢气的质量.
故答案为:
①完全反应后生成的固体的质量;②有;③充分反应后生成的氢气的质量(体积).
点评 本题以从海水中提取镁为背景,考查物质的分离、提纯,节能减排等知识,培养了学生运用知识的能力.

 阅读快车系列答案
阅读快车系列答案| A. | 场馆中使用的大量钢材属于金属材料 | |
| B. | 制造足球所用的材料都属于天然高分子材料 | |
| C. | 可用燃烧法鉴别运动员服装是否是纯棉制品 | |
| D. | 路灯的塑料灯罩属于合成材料 |
①区别硬水软水加肥皂水;
②在化学反应中只有燃烧才能放出热量;
③有单质和化合物生成的反应一定是置换反应;
④最外层电子数为8的粒子不一定是稀有气体的原子;
⑤利用铜、铁、AgN03,液能探究出铜、铁、银的金属活动性顺序;
⑥石油、煤、天然气都是不可再生的化石燃料等.
其中正确的是( )
| A. | ①④⑥ | B. | ①③④ | C. | ⑤⑥ | D. | ②⑤⑥ |
| A. | 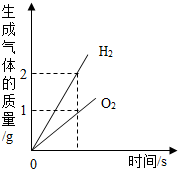 水的电解 | |
| B. |  用等质量、等浓度的过氧化氢溶液分别在加和没加MnO2条件下制取氧气 | |
| C. |  等质量的锌、铁与足量的稀硫酸反应,产生氢气的质量与反应时间的关系 | |
| D. |  某温度下,向不饱和氯化钠溶液中加入氯化钠 |
(1)观察下列图表,氧元素在人体、海水、空气地壳4种体系中,质量分数由高到低的顺序为海水、人体、地壳、空气(填4种体系的名称).
人体主要元素含量表
| 元素名称 | 质量分数/% |
| 氧 | 65.0 |
| 氮 | 18.0 |
| 氢 | 10.0 |
| 氦 | 3.0 |
| 钙 | 2.0 |
| 元素名称 | 质量分数/% |
| 氧 | 86.0 |
| 氢 | 10.3 |
| 氦 | 1.8 |
| 钠 | 1.0 |
| 镁 | 0.13 |

(2)如图是自然界中氧的部分循环示意图.从①~⑥中选择序号填空,消耗氧气的有①②④⑤,产生氧气的有③⑥.

(3)下列说法中正确的是b、e(填字母标号).
a.空气中的氧气含量永远不变;
b.空气中的氧处于动态平衡;
c.空气中氧气的浓度越高越好;
d.氧气有百利而无一害;
e.氧在自然界中既有单质,又有化合物.
| A. | 分子可以构成物质,而原子只能构成分子 | |
| B. | 在化学变化中,分子可以分成原子,而原子不能再分 | |
| C. | 在原子中,质子等于核外电子数 | |
| D. | 当原子失去或者得到电子后,其性质发生了改变 |

 如图是用红磷燃烧法来测定空气中氧气的体积分数的实验,请回答下列问题.(1)写出红磷在空气中燃烧的符号表达式4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
如图是用红磷燃烧法来测定空气中氧气的体积分数的实验,请回答下列问题.(1)写出红磷在空气中燃烧的符号表达式4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.