题目内容
17.下列实验设计不可行的是( )| A. | 加适量稀硫酸以除去硫酸钠溶液中的氢氧化钠 | |
| B. | 用稀盐酸除去铜粉中的镁粉 | |
| C. | 将氧气和氢气的混合气体通过灼热的氧化铜以除去氢气 | |
| D. | 在不用指示剂的情况下,选用CaCO3粉末将含有盐酸的CaCl2溶液调至pH=7 |
分析 A、根据硫酸可以和氢氧化钠反应生成硫酸钠进行分析;
B、根据盐酸只能和金属活动顺序表中H前面的金属反应进行分析;
C、根据可燃性的气体与氧气接触加热时可能发生爆炸进行分析;
D、根据碳酸钙可和盐酸反应生成氯化钙进行分析.
解答 解:A、硫酸可和氢氧化钠发生中和反应,生成硫酸钠,可以除去氢氧化钠,但硫酸不能过量避免引入新的杂质,故A设计可行.
B、稀盐酸和镁粉发生反应Mg+2HCl=MgCl2+H2↑,而铜不活泼,不会和盐酸反应,所以可用盐酸除去铜粉中的镁粉,故B设计可行.
C、可燃性的气体与氧气接触加热时可能发生爆炸,氢气具有可燃性,将氧气和氢气的混合气体通过灼热的氧化铜时可能发生爆炸,故C设计不合理.
D、加入CaCO3粉末发生反应CaCO3+2HCl=CaCl2+CO2↑+H2O,而CaCl2溶液呈中性,所以在不用指示剂的情况下,选用CaCO3粉末可将含有盐酸的CaCl2溶液调至pH=7,故D设计可行.
故选C.
点评 本题主要考查了学生设计实验的能力,同时考查了学生除杂题型试剂选择的依据.一般除杂试题试剂的选择要求坚持“不增、不减、过量”的原则.

练习册系列答案
相关题目
7.地壳中含量最多的金属元素是( )
| A. | Si | B. | Fe | C. | Na | D. | Al |
2.下列生活中发生的变化,属于物理变化的是( )
| A. | 死灰复燃 | B. | 冰雪融化 | C. | 铜器生锈 | D. | 食物腐败 |
9.学习化学是为了形成正确的化学观.下列有关化学的观点错误的是( )
| A. | 垃圾是放错地方的资源 | |
| B. | 节能减排、低碳出行是为了更好地保护环境 | |
| C. | 焚烧秸秆不会造成雾霾 | |
| D. | 研制可降解塑料可解决白色污染问题 |
6.下列物质间的转化,在一定条件下不能一步实现的是( )
| A. | C→CO→CO2 | B. | Fe→FeCl3→Fe(OH)3 | C. | CaCO3→CO2→H2CO3 | D. | CaO→Ca(OH)2→CaCO3 |
7. 如图是 a、b、c三种物质的溶解度曲线.请回答:
如图是 a、b、c三种物质的溶解度曲线.请回答:
(1)当a中混有少量c时,可用降温结晶(或冷却热饱和溶液)方法提纯a;
(2)若将40℃三种物质的饱和溶液分别降到20℃时,则三种溶液中溶质的质量分数大小的顺序是D(填写选项序号)
A.b>a=c B.a=b>c
C.a>b>c D.b>a>c
(3)40℃时,等质量的a、b、c三种物质的饱和溶 液中a的溶剂最少.
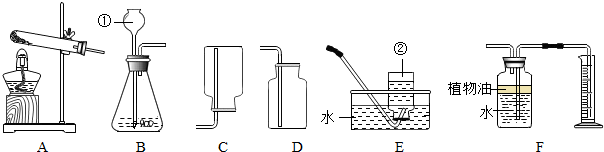
(4)用固体配制一定溶质质量分数的溶液,下列仪器中需要用到的是B
A、②④⑥⑦B、①④⑤⑥C、①③⑤⑦D、①③④⑥
(5)如图⑦较长时间放置会导致酒精挥发,酒精灯不能被点燃.
 如图是 a、b、c三种物质的溶解度曲线.请回答:
如图是 a、b、c三种物质的溶解度曲线.请回答:(1)当a中混有少量c时,可用降温结晶(或冷却热饱和溶液)方法提纯a;
(2)若将40℃三种物质的饱和溶液分别降到20℃时,则三种溶液中溶质的质量分数大小的顺序是D(填写选项序号)
A.b>a=c B.a=b>c
C.a>b>c D.b>a>c
(3)40℃时,等质量的a、b、c三种物质的饱和溶 液中a的溶剂最少.
(4)用固体配制一定溶质质量分数的溶液,下列仪器中需要用到的是B
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
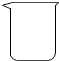 |  | 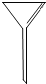 |  |  |  | 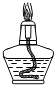 |
(5)如图⑦较长时间放置会导致酒精挥发,酒精灯不能被点燃.