题目内容
7. 如图是 a、b、c三种物质的溶解度曲线.请回答:
如图是 a、b、c三种物质的溶解度曲线.请回答:(1)当a中混有少量c时,可用降温结晶(或冷却热饱和溶液)方法提纯a;
(2)若将40℃三种物质的饱和溶液分别降到20℃时,则三种溶液中溶质的质量分数大小的顺序是D(填写选项序号)
A.b>a=c B.a=b>c
C.a>b>c D.b>a>c
(3)40℃时,等质量的a、b、c三种物质的饱和溶 液中a的溶剂最少.
(4)用固体配制一定溶质质量分数的溶液,下列仪器中需要用到的是B
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
 |  |  |  |  |  |  |
(5)如图⑦较长时间放置会导致酒精挥发,酒精灯不能被点燃.
分析 (1)根据a物质的溶解度随温度升高而增大,c物质的溶解度随温度的升高而减小进行解答;
(2)根据三种物质的溶解度随温度的变化情况及饱和溶液中溶质的质量分数计算方法进行解答;
(3)根据该温度下三种物质的溶解度曲线大小及溶解度概念进行解答;
(4)根据配制一定溶质质量分数的溶液所需仪器分析解答;
(5)根据酒精易挥发进行解答.
解答 解:(1)a物质的溶解度随温度升高而增大,c物质的溶解度随温度的升高而减小,所以当a中混有少量c时,可用冷却热饱和溶液或降温结晶的方法提纯a;
(2)若将40℃三种物质的饱和溶液分别降到20℃时,ab溶解度减小会析出晶体,溶质的质量分数减小,c的溶解度变大,溶质、溶剂的质量不变,溶质的质量分数与降温前相同;饱和溶液中溶质的质量分数的计算式$\frac{溶解度}{溶解度+100g}$×100%,即溶解度越大质量分数也就越大,而20℃时b的溶解度大于a的溶解度大于40℃时c的溶解度,所以三种溶液中溶质的质量分数大小的顺序是b>a>c;
(3)40℃时三种物质的溶解度中a最大,即等质量的水中溶解的a最多,所以等质量的a、b、c三种物质的饱和溶液中含有a溶质最多,溶剂最少;
(4)用固体配制一定溶质质量分数的溶液,需要的仪器有烧杯、药匙、托盘天平、量筒、胶头滴管、玻璃棒,故选B;
(5)因为酒精易挥发,酒精灯的忘记盖上灯帽灯帽,灯心上的酒精就会挥发掉,剩下水,很难点燃;
故答案为:(1)降温结晶(或冷却热饱和溶液);(2)D;(3)a;(4)B;(5)酒精挥发,酒精灯不能被点燃.
点评 本题难度不大,主要考查了固体溶解度曲线所表示的意义等知识,通过本题可以加强学生对固体溶解度、及饱和溶液中溶解度大则溶质质量分数大等知识的理解,培养学生应用知识解决问题的能力.

 阅读快车系列答案
阅读快车系列答案| A. | 加适量稀硫酸以除去硫酸钠溶液中的氢氧化钠 | |
| B. | 用稀盐酸除去铜粉中的镁粉 | |
| C. | 将氧气和氢气的混合气体通过灼热的氧化铜以除去氢气 | |
| D. | 在不用指示剂的情况下,选用CaCO3粉末将含有盐酸的CaCl2溶液调至pH=7 |
| 温度/℃ | 0 | 20 | 40 | 60 |
| 溶解度/g | 27.6 | 34.0 | 40.0 | 45.5 |
| A. | KCl饱和溶液中不能再溶解其他物质 | |
| B. | 20℃时,100 g饱和KCl溶液中含KCl 34.0 g | |
| C. | 20℃时,KCl溶液中溶质的质量分数一定小于40℃时溶液中溶质的质量分数 | |
| D. | 60℃时将溶质质量分数为30%的KCl溶液降温至40℃时,有晶体析出 |
| A. | 石蜡融化 | B. | 胆矾研碎 | C. | 水的蒸馏 | D. | 水的电解 |
| A. | 冰水混合物 熟石灰 | B. | 干冰 澄清石灰水 | ||
| C. | 碘酒 盐酸 | D. | 天然气 金刚石 |
| A. | “干冰”升华 | B. | 轮胎爆炸 | C. | 食物腐败 | D. | 酒精挥发 |
(1)下列各类食物中含有丰富蛋白质的是a(填写字母序号);
a.鸡蛋;b.苹果;c.白菜;d.面条
(2)如今家庭厨房中的“柴”趋向洁净,你家中的清洁能源主要有天然气.(答一种)
(3)厨房常用的塑料包装袋主要由聚乙烯或聚氯乙烯为原料制作的,其中不能用作包装食品的塑料是聚氯乙烯.
(4)下表为某品牌燕麦片标签中的一部分,根据下列标签回答问题:
| 每100g含有营养成分 | 糖类 | 油脂 | 蛋白质 | 维生素C | 钙 | 钠 | 锌 |
| 7.6g | 7.8g | 7.4g | 18mg | 201mg | 30.8mg | 8.1mg |
(5)下列所示的各种炊具、餐具中,主要利用有机合成 材料制成的是b(填写字母序号).


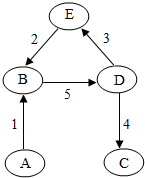 已知A、B、C、D、E是初中化学涉及到的五种物质,它们之间的关系如图所示.
已知A、B、C、D、E是初中化学涉及到的五种物质,它们之间的关系如图所示.