题目内容
8.下列说法正确的是( )| A. | 某物质在空气中中燃烧生成二氧化碳和水,证明该物质含有碳、氢、氧三种元素 | |
| B. | 盐和碱中都含有金属元素 | |
| C. | 两种物质相互反应生成盐和水,证明该反应是中和反应 | |
| D. | 一定温度下,往氢氧化钙饱和溶液中加入氧化钙,溶质、溶剂的质量的一定改变 |
分析 A、根据质量守恒定律,反应前后元素种类不变,进行分析判断.
B、根据盐和碱的特征,进行分析判断.
C、中和反应是酸与碱作用生成盐和水的反应,反应物是酸和碱,生成物是盐和水,进行分析判断.
D、根据氧化钙与水反应生成氢氧化钙,进行分析判断.
解答 解:A、某物质在空气中中燃烧生成二氧化碳和水,CO2和H2O两种物质中含有碳、氢、氧三种元素,根据质量守恒定律,反应前后,元素种类不变,反应物氧气中只含有氧元素,则该物质一定含有碳、氢两种元素,可能含有氧元素,故选项说法错误.
B、盐和碱中都不一定含有金属元素,如NH4NO3、NH3•H2O分别属于盐和碱,均不含金属元素,故选项说法错误.
C、两种物质相互反应生成盐和水,该反应不一定是中和反应,如CO2+2NaOH═Na2CO3+H2O,故选项说法错误.
D、一定温度下,往氢氧化钙饱和溶液中加入氧化钙,氧化钙与水反应生成氢氧化钙,溶剂的质量减少,有氢氧化钙析出,溶质、溶剂的质量的一定改变,故选项说法正确.
故选:D.
点评 本题难度不大,掌握中和反应的特征、质量守恒定律、盐和碱的特征等并能灵活运用是正确解答本题的关键.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
10.请根据下列实验回答问题:
(1)溶液②的质量为131.6g,属于不饱和溶液的是①(填序号).
(2)将一块塑料板放入50°C的硝酸钾饱和溶液中,塑料板漂浮于液面上.若将溶液降温到20°C时,可观察到的现象是塑料板下沉,有晶体析出.若要看到20°C的溶液中的塑料板上浮,应采用的方法是加入其他可溶性物质.
| 实验操作 | 实验结果 |
| 取100ml水,加入25g硝酸钾,搅拌 | 全部溶解,得溶液① |
| 再加10g硝酸钾,搅拌,还有3.4g固体不溶 | 得溶液② |
(2)将一块塑料板放入50°C的硝酸钾饱和溶液中,塑料板漂浮于液面上.若将溶液降温到20°C时,可观察到的现象是塑料板下沉,有晶体析出.若要看到20°C的溶液中的塑料板上浮,应采用的方法是加入其他可溶性物质.
3.在研究酸和碱的化学性质时,同学们想证明:稀H2SO4与NaOH溶液确实发生了反应.请你与他们一起完成实验方案设计、实施和评价.(注:硫酸钠溶液呈中性)
(1)向NaOH溶液中滴入2-3滴酚酞溶液,溶液由无色变为红色.

(2)根据上述实验中颜色变化,确定稀H2SO4与NaOH溶液发生了化学反应,反应的化学方程式为H2SO4+2NaOH═Na2SO4+2H2O.
(3)因为溶液变成了无色,小林说“稀硫酸一定过量了”,小林这么说的理由是酸溶液不能使酚酞溶液变色.
(4)为确定小林的说法是否正确,同学们又设计了下列实验方案并进行实验:
上述方案中,你认为正确的是方案二(填“方案一”或“方案二”).
另外一个实验方案错误的原因(用化学方程式表示):BaCl2+Na2SO4═BaSO4↓+2NaCl.
请你再设计一种实验方案确定稀H2SO4过量,你选用铁粉(填药品).
(1)向NaOH溶液中滴入2-3滴酚酞溶液,溶液由无色变为红色.

(2)根据上述实验中颜色变化,确定稀H2SO4与NaOH溶液发生了化学反应,反应的化学方程式为H2SO4+2NaOH═Na2SO4+2H2O.
(3)因为溶液变成了无色,小林说“稀硫酸一定过量了”,小林这么说的理由是酸溶液不能使酚酞溶液变色.
(4)为确定小林的说法是否正确,同学们又设计了下列实验方案并进行实验:
| 实验方案 | 实验步骤 | 实验现象 | 实验结论 |
| 方案一 | 取样,滴入适量的氯化钡溶液 | 出现白色沉淀 | 稀H2SO4过量 |
| 方案二 | 取样,滴入2-3滴紫色石蕊溶液 | 溶液变成红色 | 稀H2SO4过量 |
另外一个实验方案错误的原因(用化学方程式表示):BaCl2+Na2SO4═BaSO4↓+2NaCl.
请你再设计一种实验方案确定稀H2SO4过量,你选用铁粉(填药品).
13.厨房里发生的下列变化,属于物理变化的是( )
| A. | 蔬菜腐烂 | B. | 木炭燃烧 | C. | 水的沸腾 | D. | 菜刀生锈 |
18.如图为甲、乙两种物质的溶解度曲线,下列说法不正确的是( )
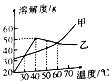

| A. | 30℃时,甲、乙的溶解度相同 | |
| B. | 将甲的溶液降温,一定有晶体析出 | |
| C. | 40℃时,乙饱和溶液比甲饱和溶液溶质质量分数大 | |
| D. | 甲、乙都属于易溶物质 |




 甲和乙两种物质的溶解度曲线如图所示:
甲和乙两种物质的溶解度曲线如图所示: