题目内容
1.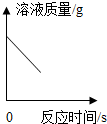 下列各组物质中,能相互反应且反应前后溶液总质量随时间变化符合如图所示的是( )
下列各组物质中,能相互反应且反应前后溶液总质量随时间变化符合如图所示的是( )| A. | 铁和硝酸银溶液 | B. | 硫酸和烧碱溶液 | ||
| C. | 氧化铜和盐酸 | D. | 硝酸钾溶液和稀硫酸 |
分析 如果是置换反应关键看置换出来的是什么,根据进入溶液中的质量与置换出来的质量之差考虑,如果不是置换反应就看反应后生成物的质量变化,反应后生成气体和沉淀的溶液质量减轻.
解答 解:A、铁和硝酸银溶液反应生成物是银和硝酸亚铁,进入溶液中的是铁相对原子质量为56,置换出来的是银的相对原子质量为108,则进入的少,出来得多,所以溶液质量减少了,故正确;
B、硫酸和烧碱溶液生产硫酸钠和水,溶液质量不变,故错误;
C、氧化铜固体和盐酸反应生成氯化铁和水,溶液质量增加,故错误;
D、硝酸钾溶液和稀硫酸不反应,溶液质量不变,故错误;
故选:A.
点评 解答本题的主要方法是看进入溶液中的物质是什么,被置换出来的物质是什么,根据二者的差值来分析溶液的质量变化情况.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
12. 硝酸铜是制备Cu-Zn-Al系催化剂的重要原料,某兴趣小组对它开展了以下研究.
硝酸铜是制备Cu-Zn-Al系催化剂的重要原料,某兴趣小组对它开展了以下研究.
(1)硝酸铜的制备研究
该小组同学查阅资料发现有三种设计方案可供选用:
①Cu与稀硝酸反应制取:3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O
②Cu与浓硝酸反应制取:Cu+4HNO3═Cu(NO3)2+2NO2↑+2H2O
③通氧气于铜屑与稀硝酸的体系中制取:2Cu+4HNO3+O2═2Cu(NO3)2+2H2O
甲同学认为三种方案的反应都可以在铁制容器中进行,乙同学认为不可行(填“可行”“不
可行”),理由是(用一个化学方程式表示)Fe+Cu(NO3)2═Cu+Fe(NO3)2.从环境保护和经济效益角度考虑,制取大量的硝酸铜最宜采用以上方法③,理由是①②产生污染空气的有害气体,③中反应过程没有有毒气体生成,不污染环境,硝酸利用率高.
(2)硝酸铜的性质研究
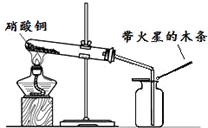
硝酸铜为蓝色固体,溶于水可得蓝色溶液.该小组同学用如图装置加热硝酸铜,发现固体由蓝色逐渐变黑,同时产生红棕色有刺激性气味的气体,带火星的木条复燃.
【提出问题】硝酸铜在加热条件下到底发生了怎样的反应?
【查阅资料】
①氧化铜和稀硫酸反应的化学方程式:CuO+H2SO4═CuSO4+H2O
②含氮化合物中,只有NO2是红棕色、有刺激性气味的气体.
③NO2有助燃性,能使带火星的木条复燃
【猜想假设】
Cu(NO3)2受热分解除了生成NO2,还可能生成了CuO和O2.
【进行实验】
步骤II是同学们查阅了新的资料后设计完成的.该资料是关于NO2的沸点(或低温下NO2能否反应生成液态或固态物质)方面的性质信息.
【获得结论】根据实验结果,Cu(NO3)2受热分解的化学方程式为2Cu(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+4NO2↑+O2↑.
该小组同学取10g的硝酸铜加热一段时间后,测得剩余固体的质量为4.6g,则硝酸铜的分解率为9.2%?(分解率为已分解的硝酸铜占原硝酸铜的质量分数,写出计算过程)
【反思与评价】
已知相同状况下,气体的体积比等于其分子个数比.据此,同学们认为,即使没有资料③,依据实验结论和“加热硝酸铜产生的气体能使带火星的木条复燃”的实验现象,也能推出NO2可能具有助燃性.理由是硝酸铜分解生成的气体中NO2与O2的体积比为4:1,O2所占的体积分数与空气中O2的体积分数相同,分解生成气体能使带火星木条复燃而空气不能,说明NO2有助燃性.
 硝酸铜是制备Cu-Zn-Al系催化剂的重要原料,某兴趣小组对它开展了以下研究.
硝酸铜是制备Cu-Zn-Al系催化剂的重要原料,某兴趣小组对它开展了以下研究.(1)硝酸铜的制备研究
该小组同学查阅资料发现有三种设计方案可供选用:
①Cu与稀硝酸反应制取:3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O
②Cu与浓硝酸反应制取:Cu+4HNO3═Cu(NO3)2+2NO2↑+2H2O
③通氧气于铜屑与稀硝酸的体系中制取:2Cu+4HNO3+O2═2Cu(NO3)2+2H2O
甲同学认为三种方案的反应都可以在铁制容器中进行,乙同学认为不可行(填“可行”“不
可行”),理由是(用一个化学方程式表示)Fe+Cu(NO3)2═Cu+Fe(NO3)2.从环境保护和经济效益角度考虑,制取大量的硝酸铜最宜采用以上方法③,理由是①②产生污染空气的有害气体,③中反应过程没有有毒气体生成,不污染环境,硝酸利用率高.
(2)硝酸铜的性质研究
硝酸铜为蓝色固体,溶于水可得蓝色溶液.该小组同学用如图装置加热硝酸铜,发现固体由蓝色逐渐变黑,同时产生红棕色有刺激性气味的气体,带火星的木条复燃.
【提出问题】硝酸铜在加热条件下到底发生了怎样的反应?
【查阅资料】
①氧化铜和稀硫酸反应的化学方程式:CuO+H2SO4═CuSO4+H2O
②含氮化合物中,只有NO2是红棕色、有刺激性气味的气体.
③NO2有助燃性,能使带火星的木条复燃
【猜想假设】
Cu(NO3)2受热分解除了生成NO2,还可能生成了CuO和O2.
【进行实验】
| 实验操作 | 实验现象 | 实验结论 |
| 步骤I:将反应后试管中的固体加水充分溶解,过 滤,向滤渣中加入足量稀硫酸,加热 | 固体全部溶解,得到蓝色溶液 | 硝酸铜分解生成了氧化铜. |
步骤II:在如图的试管和集气瓶之间连上此图所示的装置,重新进行加热硝酸铜的实验 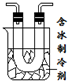 | 集气瓶中气体为无色,带火星的木条复燃 带火星的木条复燃 | 硝酸铜分解生成了氧气 |
【获得结论】根据实验结果,Cu(NO3)2受热分解的化学方程式为2Cu(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+4NO2↑+O2↑.
该小组同学取10g的硝酸铜加热一段时间后,测得剩余固体的质量为4.6g,则硝酸铜的分解率为9.2%?(分解率为已分解的硝酸铜占原硝酸铜的质量分数,写出计算过程)
【反思与评价】
已知相同状况下,气体的体积比等于其分子个数比.据此,同学们认为,即使没有资料③,依据实验结论和“加热硝酸铜产生的气体能使带火星的木条复燃”的实验现象,也能推出NO2可能具有助燃性.理由是硝酸铜分解生成的气体中NO2与O2的体积比为4:1,O2所占的体积分数与空气中O2的体积分数相同,分解生成气体能使带火星木条复燃而空气不能,说明NO2有助燃性.
16.在人类所需的营养素中属于维持生命活动的备用能源,且摄入过多会引起肥胖的是( )
| A. | 维生素 | B. | 油脂 | C. | 蛋白质 | D. | 无机盐 |
13.你喜欢烹饪吗?高超的烹饪技艺不仅能改善营养,而且能丰富生活情趣,下列烹饪的菜肴中富含油脂的是( )
| A. | 凉拌黄瓜 | B. | 清蒸螃蟹 | C. | 玉米窝头 | D. | 红烧肥肉 |
10.如图实验装置不能达到相应实验目的装置是( )
| A. |  除去一氧化碳中的二氧化碳 | B. |  排水法收集氧气 | ||
| C. |  向上排空气法收集氧气 | D. |  检验氮气中是否含有氯化氢 |
11.下列关于物质的分类正确的是( )
| A. | 单质:石墨、水银、液氮 | B. | 碱:烧碱、纯碱、氢氧化铜 | ||
| C. | 混合物:食醋、盐水、金刚石 | D. | 有机物:蛋白质、乙醇、糖水 |

 如图A、B、C为三种物质的溶解度曲线,据图回答:
如图A、B、C为三种物质的溶解度曲线,据图回答: