题目内容
12.将25g石灰石样品放入烧杯中(杂质既不溶于水也不参加反应),加入稀盐酸至恰好完全反应,共用去稀盐酸100g.烧杯内剩余物质的总质量为116.2g.请计算:(1)生成二氧化碳的质量为8.8 g.
(2)反应后所得溶液中溶质质量分数为多少?(结果保留至1%)
分析 碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,由质量守恒定律,烧杯内质量的减少的质量即生成的二氧化碳的质量,据此根据反应的化学方程式列式计算出生成氯化钙的质量,进而计算出反应后所得溶液中溶质质量分数.
解答 解:(1)由质量守恒定律,生成二氧化碳的质量为25g+100g-116.2g=8.8g.
(2)设生成氯化钙的质量为x,参加反应的碳酸钙的质量为y
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 111 44
y x 8.8g
$\frac{111}{44}=\frac{x}{8.8g}$ x=22.2g
$\frac{100}{44}=\frac{y}{8.8g}$ y=20g
反应后所得溶液中溶质质量分数为$\frac{22.2g}{20g+100g-8.8g}$×100%≈20%.
故答案为:(1)8.8;(2)反应后所得溶液中溶质质量分数为20%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,根据质量守恒定律计算出二氧化碳的质量是正确解答本题的前提和关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.下列叙述正确的是( )
| A. | 浓溶液不一定是饱和溶液,稀溶液也不一定是不饱和溶液 | |
| B. | 20℃时,36g氯化钠溶于100g水中,恰好达到饱和,此溶液中溶质的质量分数是36% | |
| C. | 温度升高时,物质的溶解度增大 | |
| D. | 凡是均一,透明的液体就是溶液 |
1.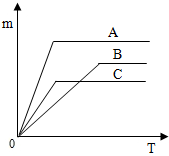 等质量的A、B、C三种金属与足量的稀硫酸反应后生成+2价的硫酸盐,生成氢气的质量(m)与反应时间(T)的关系图如图所示,则下列说法正确的( )
等质量的A、B、C三种金属与足量的稀硫酸反应后生成+2价的硫酸盐,生成氢气的质量(m)与反应时间(T)的关系图如图所示,则下列说法正确的( )
 等质量的A、B、C三种金属与足量的稀硫酸反应后生成+2价的硫酸盐,生成氢气的质量(m)与反应时间(T)的关系图如图所示,则下列说法正确的( )
等质量的A、B、C三种金属与足量的稀硫酸反应后生成+2价的硫酸盐,生成氢气的质量(m)与反应时间(T)的关系图如图所示,则下列说法正确的( )| A. | 三种金属的相对原子量是A<C<B | B. | 三种金属的活泼性是A>B>C | ||
| C. | 反应消耗硫酸的质量相同 | D. | 反应速度最快的是A,最慢的是B |

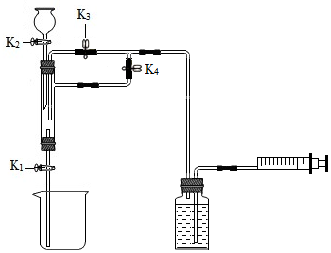 甲、乙两个实验小组利用如图装置(夹持装置已略去),做了一个兴趣实验,证明了二氧化碳与氢氧化钠的反应产物中有碳酸钠生成.他们的实验步骤如下:
甲、乙两个实验小组利用如图装置(夹持装置已略去),做了一个兴趣实验,证明了二氧化碳与氢氧化钠的反应产物中有碳酸钠生成.他们的实验步骤如下: 2015年,为推进“惠民”工程,哈尔滨市正在进行市容市貌的升级工作,针对重要窗口的路灯进行改造,部分道路的两侧使用了一些太阳能路灯.
2015年,为推进“惠民”工程,哈尔滨市正在进行市容市貌的升级工作,针对重要窗口的路灯进行改造,部分道路的两侧使用了一些太阳能路灯.