题目内容
17.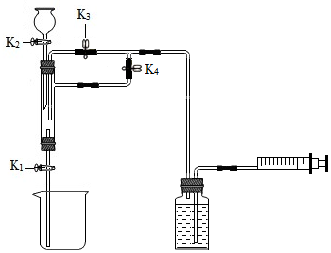 甲、乙两个实验小组利用如图装置(夹持装置已略去),做了一个兴趣实验,证明了二氧化碳与氢氧化钠的反应产物中有碳酸钠生成.他们的实验步骤如下:
甲、乙两个实验小组利用如图装置(夹持装置已略去),做了一个兴趣实验,证明了二氧化碳与氢氧化钠的反应产物中有碳酸钠生成.他们的实验步骤如下:①在玻璃管中加入一定量碳酸钙,关闭K1、K3,打开K4,从分液漏斗放入稀盐酸并收集二氧化碳
②打开K1,使玻璃管中的液体流入烧杯,并用清水冲洗
③关闭K1,从分液漏斗向玻璃管中加入氢氧化钠溶液
④使二氧化碳与氢氧化钠充分反应
⑤关闭K3,打开K4,从分液漏斗放入稀盐酸
⑥打开K1,使玻璃管中的液体流入烧杯
回答下列问题:
(1)步骤①中发生反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O.
(2)步骤④的具体操作是关闭K3,打开K4,推动注射器活塞使液体进入集气瓶,并将二氧化碳压入玻璃管内.
(3)整个过程中注射器的作用是容纳集气瓶内液体,排除气体.
(4)在步骤⑥中,甲乙两组观察到了不同的现象.甲组发现烧杯中液体变浑浊;乙组发现烧杯中产生了大量气泡.两组产生不同现象的原因是步骤①中所加盐酸的量不同,甲组同学所用盐酸适量,而乙组同学所用盐酸过量.
分析 (1)根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳进行分析;
(2)根据步骤④的具体操作是将集气瓶内的二氧化碳压入玻璃管内与氢氧化钠进行分析;
(3)根据整个过程中注射器的作用是容纳集气瓶内液体,排除气体进行分析;
(4)根据反应物的量不同,产生的现象也不相同进行分析.
解答 解:(1)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O;
(2)步骤④的具体操作是将集气瓶内的二氧化碳压入玻璃管内与氢氧化钠,所以步骤④的具体操作是:关闭K3,打开K4,推动注射器活塞使液体进入集气瓶,并将二氧化碳压入玻璃管内;
(3)整个过程中注射器的作用是容纳集气瓶内液体,排除气体;
(4)反应物的量不同,产生的现象也不相同,甲组中氯化钙和碳酸钠反应生成碳酸钙沉淀,乙组中盐酸和碳酸钠反应生成二氧化碳气体,所以在步骤⑥中,甲乙两组观察到了不同的现象.甲组发现烧杯中液体变浑浊;乙组发现烧杯中产生了大量气泡.两组产生不同现象的原因是步骤①中所加盐酸的量不同,甲组同学所用盐酸适量,而乙组同学所用盐酸过量.
故答案为:(1)CaCO3+2HCl=CaCl2+CO2↑+H2O;
(2)关闭K3,打开K4,推动注射器活塞使液体进入集气瓶,并将二氧化碳压入玻璃管内;
(3)容纳集气瓶内液体,排除气体;
(4)步骤①中所加盐酸的量不同,甲组同学所用盐酸适量,而乙组同学所用盐酸过量.
点评 两种物质反应,反应后的溶液中除了要考虑生成物之外,还要考虑反应物是否有剩余.

练习册系列答案
相关题目
8.同学们从山上采集到一种石灰石,他们取80克该样品加入100克的稀盐酸进行实验(所含杂质不溶于水也不和稀盐酸反应),每隔一段时间测定烧杯内剩余物质质量.测得烧杯内剩余物质的质量(m)与反应时间(t)的关系如下表:
请回答下列问题:
(1)当石灰石完全反应后,生成CO2的质量为22g.
(2)求该石灰石中CaCO3的质量分数,写出计算过程.
| 反应时间t∕s | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
| 反应后物质质量m∕g | 180 | 175 | 170 | 166 | 162 | 158 | 158 |
(1)当石灰石完全反应后,生成CO2的质量为22g.
(2)求该石灰石中CaCO3的质量分数,写出计算过程.
5.分别将5g下列物质加入95g水中,所得溶液质量分数最小的是( )
| A. | 氢氧化钙 | B. | 硫酸铜晶体(CuSO4•5H2O) | ||
| C. | 氧化钠 | D. | 氯化钠 |
9.下列归纳和总结完全正确的一组是( )
| A.对除杂的认识 | B.鉴别的方法 |
| ①用化学方法除去食盐水中可溶性杂质 ②用磁铁除去铁粉中木炭粉 ③用碳酸钠除去CaCl2溶液中的HCl | ①用燃着的木条鉴别氧气和二氧化碳 ②用熟石灰区别化肥硝酸钾和硝酸铵 ③用酚酞试液鉴别稀盐酸和氯化钠溶液 |
| C.对现象的认识 | D.化学学与贡献 |
| ①花香四溢,说明分子在不断运动 ②镁条燃烧,有大量白雾产生 ③电解水生成氢气和氧气的体积比为2:1 | ①拉瓦锡-发现空气的主要成分 ②门捷列夫-发现元素周期表 ③侯德榜-发明联合制碱法 |
| A. | A | B. | B | C. | C | D. | D |
6.下列有关物质的化学式、名称、俗名对应错误的是( )
| A. | NaHCO3 碳酸氢钠 小苏打 | B. | CaO 氧化钙 熟石灰 | ||
| C. | Na2CO3 碳酸钠 纯碱 | D. | NaOH 氢氧化钠 烧碱 |
 电烤箱越来越多的进入了哈尔滨人的生活,亲手为家人做出健康美味的食品变得简单.电烤箱内上下各有几根不锈钢的加热管,能用不锈钢做加热管,是因为不锈钢具有导热性好(写一条即可)的物理性质,电烤箱在工作过程中的能量转化为电能转化为热能;在烘焙糕点时所用的发酵粉的重要成分之一是小苏打,使烘焙的糕点松软可口.制作糕点时,部分小苏打是通过受热分解产生二氧化碳气体使面蓬松,同时产生苏打和水,该反应的化学方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,该反应中,没有发生化合价变化的元素有4种.
电烤箱越来越多的进入了哈尔滨人的生活,亲手为家人做出健康美味的食品变得简单.电烤箱内上下各有几根不锈钢的加热管,能用不锈钢做加热管,是因为不锈钢具有导热性好(写一条即可)的物理性质,电烤箱在工作过程中的能量转化为电能转化为热能;在烘焙糕点时所用的发酵粉的重要成分之一是小苏打,使烘焙的糕点松软可口.制作糕点时,部分小苏打是通过受热分解产生二氧化碳气体使面蓬松,同时产生苏打和水,该反应的化学方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,该反应中,没有发生化合价变化的元素有4种.