题目内容
12.亚硝酸钠(NaNO2)常用作食品的发色剂和防腐剂,但食品中的亚硝酸钠含量超标会危害人体健康.亚硝酸钠具有咸味,外形和食盐很相似,亚硝酸钠的水溶液呈碱性.建筑行业常用亚硝酸钠作水泥添加剂.近年来,在建筑工地多次发生误将亚硝酸钠当作食盐食用导致中毒的事件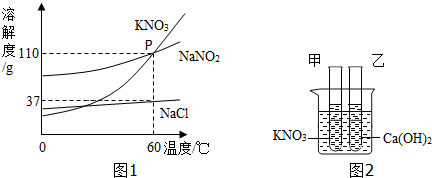
(1)请设计方案鉴别氯化钠和亚硝酸钠两种固体物质,简要说明实验操作步骤、发生的现象及结论实验步骤:把两种物质分别溶解在水中,配成溶液,再分别向两种溶液中滴加硝酸银溶液;
实验现象:一种溶液中无明显现象,一种溶液中有白色沉淀生成;
实验结论:无明显现象的溶液中,原物质是亚硝酸钠,有白色沉淀生成的溶液中,原物质是氯化钠.
(2)如图1所示为KNO3、NaNO2(亚硝酸钠)、NaCl的溶解度曲线,请根据溶解度曲线回答下列问题:
①60℃时,KNO3的饱和溶液中溶质的质量分数等于(填“大于”、“等于”或“小于”)NaNO2饱和溶液中溶质的质量分数.
②60℃时,取NaNO2和NaCl两种固体各50g,分别加入到100g水中充分搅拌,能得到饱和溶液的物质是NaCl(填“NaNO2”或“NaCl”).
③点P的表示的一条意义是60℃时,硝酸钾和亚硝酸钠的溶解度相等.
(3)如图2所示.甲、乙两试管中分别盛有硝酸钾、氢氧化钙的饱和溶液,并都有少量固体存在.若向试管外的烧杯中加入少量浓硫酸,搅拌,充分溶解.简述你在试管中看到的实验现象,并作出合理的解释.硝酸钾固体逐渐溶解,氢氧化钙固体逐渐增多,浓硫酸溶于水,放出热量,氢氧化钙的溶解度随温度的升高而减,硝酸钾的溶解度随温度的升高而增大.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)鉴别氯化钠和亚硝酸钠两种固体物质的方法如下:
实验步骤:把两种物质分别溶解在水中,配成溶液,再分别向两种溶液中滴加硝酸银溶液;
实验现象:一种溶液中无明显现象,一种溶液中有白色沉淀生成;
实验结论:无明显现象的溶液中,原物质是亚硝酸钠,有白色沉淀生成的溶液中,原物质是氯化钠;
(2)①60℃时,KNO3的溶解度和NaNO2的溶解度相等,则该温度下KNO3的饱和溶液中溶质的质量分数等于NaNO2饱和溶液中溶质的质量分数;
②60℃时,亚硝酸钠的溶解度是110g,50g亚硝酸钠溶解在100g水中充分搅拌后,不能形成饱和溶液;
60℃时,氯化钠的溶解度是37g,50g氯化钠加入到100g水中充分搅拌后,能形成饱和溶液;
③点P的表示的一条意义是:60℃时,硝酸钾和亚硝酸钠的溶解度相等;
(3)在试管中看到的实验现象以及合理的解释是:硝酸钾固体逐渐溶解,氢氧化钙固体逐渐增多,浓硫酸溶于水,放出热量,氢氧化钙的溶解度随温度的升高而减,硝酸钾的溶解度随温度的升高而增大.
故答案为:(1)实验步骤:把两种物质分别溶解在水中,配成溶液,再分别向两种溶液中滴加硝酸银溶液;
实验现象:一种溶液中无明显现象,一种溶液中有白色沉淀生成;
(2)①等于;
②NaCl;
③60℃时,硝酸钾和亚硝酸钠的溶解度相等;
(3)硝酸钾固体逐渐溶解,氢氧化钙固体逐渐增多,浓硫酸溶于水,放出热量,氢氧化钙的溶解度随温度的升高而减,硝酸钾的溶解度随温度的升高而增大.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.


根据如图所示微观示意图得出的结论中,正确的是( )
| A. | 反应中含氢元素的化合物有三种 | |
| B. | 反应中甲和丙的质量之比为4:7 | |
| C. | 反应前后碳元素的化合价没有发生变化 | |
| D. | 水煤气的成分是一氧化碳和氧气 |
| A. |  氧炔焰焊接 | B. |  植物光合作用 | C. |  古青铜器锈蚀 | D. |  用潮汐能发电 |
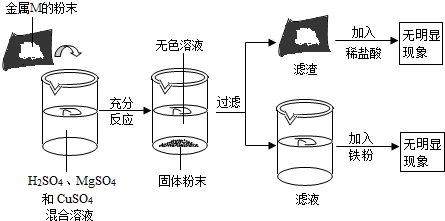
| A. | 金属M可能是单质铁 | B. | 滤渣中一定含有铜,可能含有金属M | ||
| C. | 滤液的质量大于原混合溶液的质量 | D. | 滤液中一定含有两种金属阳离子 |

| A. | B、C、D三种元素在原素周期表中位于不同的周期 | |
| B. | 当m=8时,D粒子表示氯离子 | |
| C. | A、B两种粒子具有相似的化学性质 | |
| D. | 四种粒子可能都呈电中性 |
| A. |  滴加液体 | B. |  加热液体 | C. |  闻药品气味 | D. |  稀释浓硫酸 |


