题目内容
14.焊接或切割金属常用氧炔焰.氧炔焰是乙炔(C2H2)气体和氧气反应产生的3000°C以上的高温火焰.乙炔由固体碳化钙(化学式为CaC2)与水反应制得,同时生成一种白色固体.【提出问题】白色固体是什么物质?
【进行猜想】刘平同学认为有以下几种可能:
想一:CaO;猜想二:CaCO3;猜想三:Ca(OH)2.
的依据是根据质量守恒定律.
【交流评价】经过同学交流讨论,认为猜想一成立.否定猜想一的理由是:氧化钙与水反应也生成氢氧化钙.
【交流评价】
| 实验操作 | 实验现象 | 结论 | |
| 实验一 | 取样于试管中,滴加稀盐酸 | 猜想二:不成立 | |
| 实验二 | 猜想三:成立 |
出碳化钙与水反应制取乙炔的化学方程式:CaC2+2H2O=Ca(OH)2+C2H2↑.
分析 【做出猜想】
根据质量守恒定律可知,白色固体可能是氧化钙,或碳酸钙,或氢氧化钙;
【交流反思】
氧化钙能和水反应生成氢氧化钙;
【进行实验】
碳酸钙能和稀盐酸反应生成氯化钙、水和二氧化碳;
二氧化碳能使澄清的石灰水变浑浊;
【实验结论】根据反应物和生成物利用质量守恒定律写化学方程式.
解答 解:
【做出猜想】
根据元素守恒进行猜想,他的依据是根据质量守恒定律;
故填:根据质量守恒定律;
【交流反思】
经过同学们交流讨论,认为猜想一不成立.否定猜想一的理由是:CaO能与水反应.
故填:氧化钙与水反应也生成氢氧化钙.
【进行实验】
(一)根据碳酸钙能和稀盐酸反应生成氯化钙、水和二氧化碳;如果取少量白色固体放入试管中,滴加稀盐酸,没有观察到气泡放出,则证明猜想二不成立.
(二)根据二氧化碳能使澄清的石灰水变浑浊;则取少量白色固体加入到水中,取上层清液,通入二氧化碳气体,有白色沉淀出现,证明猜想三成立.该反应的化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O.
【实验结论】碳化钙与水反应制取乙炔的化学方程式CaC2+2H2O=Ca(OH)2+C2H2↑
故答案:
【做出猜想】
根据质量守恒定律;
【交流反思】氧化钙与水反应也生成氢氧化钙;
【进行实验】
(一)没气泡
(二)取少量白色固体加水溶解,取上层清液,通入二氧化碳气体
有白色沉淀出现
【实验结论】CaC2+2H2O=Ca(OH)2+C2H2↑.
点评 化学实验现象是化学实验最突出、最鲜明的部分,也是进行分析推理得出结论的依据,掌握物质的性质和相互之间的反应关系,并有助于提高观察、实验能力.所以,对化学实验不仅要认真观察,还应掌握观察实验现象的方法.

练习册系列答案
 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案 高效智能课时作业系列答案
高效智能课时作业系列答案
相关题目
13.空气是生命赖以存在的物质基础,也是人类生产活动的重要资源,下列有关空气的说法正确的是( )
| A. | 空气中分离出的氮气化学性质不活泼,可做食品保护气 | |
| B. | 空气主要是由氧气和氮气组成,其中氧气的质量约占空气质量的$\frac{1}{5}$ | |
| C. | 空气质量报告中所列的空气质量级别数值越大,说明空气的质量越好 | |
| D. | 空气中的稀有气体是一种纯净物,化学性质很稳定,常用于制造多种用途的电光源 |
14.某活动小组从工厂收集到了一些含有硝酸银的废液以及废铁屑、废锌屑的混合物,他们欲将废液中的银进行回收,把一定量的上述金属混合物加入到含硝酸银的废液中,充分反应后过滤,得到固体和浅绿色滤液.关于滤液中的溶质和固体成分猜想合理的是( )
| A. | 溶质一定含有硝酸亚铁,可能含有硝酸锌 | |
| B. | 固体中一定没有锌 | |
| C. | 溶质一定含有硝酸锌和硝酸亚铁,可能含有硝酸银 | |
| D. | 固体中一定含有银和铁 |
2.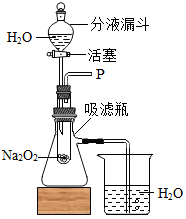 “在学校的元旦联欢会上,某同学表演了‘水能生火’的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.”
“在学校的元旦联欢会上,某同学表演了‘水能生火’的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.”
小颖看到这段话后非常感兴趣,她和同学们一起对该问题进行了一系列的探究.
[提出问题]过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
[猜 想]①可能有一种气体和另一种物质生成
②反应过程中可能有能量变化
[实验探究]实验一:探究反应后生成的气体是什么?
(1)打开图装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃.说明生成的气体是氧气;
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:过氧化钠和水反应是放热反应,使吸滤瓶内气体体积膨胀.
实验二:探究反应后生成的另一种物质是什么?
(1)小明猜想另一种物质是Na2CO3,小军认为不可能.原因是:质量守恒定律.
为了证实小军的看法,请你设计一个证明CO32-不存在的实验:
(2)小军取反应后所得的溶液于试管中,滴入无色酚酞试液,发现试管中的溶液变成红色,说明反应后所得的溶液呈碱性;
[表 达]小军根据实验探究的结果,写出了过氧化钠和水反应的化学方程式为2Na2O2+2H2O═4NaOH+O2↑.
[发现问题]小娟发现在小军的实验中,试管中的溶液变成红色后,一会儿又变成无色.
[深入探究]实验三:探究滴入无色酚酞试液后,变成红色的溶液为什么会褪色?
小娟经查阅资料,设计了如下实验方案,并将有关现象记录在下表中.
(1)根据小娟的实验探究,过氧化钠和水反应除了小军写出的反应外还存在另一个反应,其化学方程式为Na2O2+2H2O═2NaOH+H2O2.
(2)综合分析上述实验,猜想使变红的酚酞褪色的物质是H2O2,请你用实验1所得的溶液,设计一个简单实验证明你的猜想在实验1所得溶液中加入少许MnO2,直到无气体产生时,再加入无色酚酞试液,溶液变红且不再褪色.
(3)根据实验3测得的气体体积说明了水与Na2O2反应生成的H2O2约有$\frac{1}{3}$发生分解.
 “在学校的元旦联欢会上,某同学表演了‘水能生火’的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.”
“在学校的元旦联欢会上,某同学表演了‘水能生火’的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.”小颖看到这段话后非常感兴趣,她和同学们一起对该问题进行了一系列的探究.
[提出问题]过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
[猜 想]①可能有一种气体和另一种物质生成
②反应过程中可能有能量变化
[实验探究]实验一:探究反应后生成的气体是什么?
(1)打开图装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃.说明生成的气体是氧气;
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:过氧化钠和水反应是放热反应,使吸滤瓶内气体体积膨胀.
实验二:探究反应后生成的另一种物质是什么?
(1)小明猜想另一种物质是Na2CO3,小军认为不可能.原因是:质量守恒定律.
为了证实小军的看法,请你设计一个证明CO32-不存在的实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 取样品,加入稀盐酸 | 没有气泡产生 | 生成物中没有CO32- |
[表 达]小军根据实验探究的结果,写出了过氧化钠和水反应的化学方程式为2Na2O2+2H2O═4NaOH+O2↑.
[发现问题]小娟发现在小军的实验中,试管中的溶液变成红色后,一会儿又变成无色.
[深入探究]实验三:探究滴入无色酚酞试液后,变成红色的溶液为什么会褪色?
小娟经查阅资料,设计了如下实验方案,并将有关现象记录在下表中.
| 实验序号 | 实验方案 | 实验现象 |
| 1 | 将水滴入盛有过氧化钠固体的试管中,配制成溶液,用带火星的木条检验生成的气体 | 反应激烈,有大量气体产生,并能使木条复燃 |
| 2 | 取三份实验1所得溶液分装于三支试管中是进行如下实验: ①第一份中加入紫色石蕊试液 ②第二份中加入无色酚酞试液 ③第三份中先加水再加入无色酚酞试液 | ①溶液变蓝且长时间不褪色 ②溶液显红色,半分钟内褪色 ③溶液显红色,半分钟内褪色 |
| 3 | ①称取3.9g过氧化钠固体,逐滴加入约50mL水. ②待不再产生气体,10min以后,加入用小纸片包好的MnO2,迅速塞紧双孔塞,轻轻摇动反应器,纸包自动散开,MnO2与溶液开始接触. | ①测得氧气体积为185mL左右 ②又产生大量氧气,至反应完全以后,又测得产生了374mL氧气(两次测定条件均相同) |
(2)综合分析上述实验,猜想使变红的酚酞褪色的物质是H2O2,请你用实验1所得的溶液,设计一个简单实验证明你的猜想在实验1所得溶液中加入少许MnO2,直到无气体产生时,再加入无色酚酞试液,溶液变红且不再褪色.
(3)根据实验3测得的气体体积说明了水与Na2O2反应生成的H2O2约有$\frac{1}{3}$发生分解.
9.善于梳理有利于知识的系统化,以下归纳完全正确的一组是( )
| A物质的分类 | B物质的微观构成 |
| 常见的混合物--空气、溶液、合金 常见的氧化物--冰、干冰、高锰酸钾 常见合金--不锈钢、生铁、黄铜 | 铜--由铜原子构成 水--由水分子构成 氯化钠--由钠离子、氯离子构成 |
| C物质的性质与用途 | D物质的鉴别 |
| CO的还原性--可冶炼金属 O2的助燃性--可用作燃料 洗洁精的乳化用用--除去餐具油污 | 稀盐酸和水--紫色石蕊溶液 氮气和二氧化碳--带火星的木条 铁和铜--观察颜色 |
| A. | A | B. | B | C. | C | D. | D |
19.下列实验操作正确的是( )
| A. | 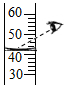 | B. | 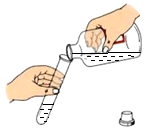 | C. | 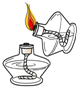 | D. | 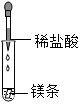 |
3.下列有关氧气的说法不正确的是( )
| A. | 分离液态空气法制取氧气,是物理变化 | |
| B. | 按质量计算,空气中含有氧气约21% | |
| C. | 铜在氧气中加热后表面会变为黑色 | |
| D. | 氧气可以作为火箭的助燃剂 |
 A、B、C、D、E、F、G为常见的物质,其中B、E、G属于单质,反应②是炼铁工业中的主要反应,下图是它们之间的相互转化关系.请回答:
A、B、C、D、E、F、G为常见的物质,其中B、E、G属于单质,反应②是炼铁工业中的主要反应,下图是它们之间的相互转化关系.请回答: