题目内容
2.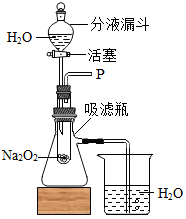 “在学校的元旦联欢会上,某同学表演了‘水能生火’的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.”
“在学校的元旦联欢会上,某同学表演了‘水能生火’的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.”小颖看到这段话后非常感兴趣,她和同学们一起对该问题进行了一系列的探究.
[提出问题]过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
[猜 想]①可能有一种气体和另一种物质生成
②反应过程中可能有能量变化
[实验探究]实验一:探究反应后生成的气体是什么?
(1)打开图装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃.说明生成的气体是氧气;
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:过氧化钠和水反应是放热反应,使吸滤瓶内气体体积膨胀.
实验二:探究反应后生成的另一种物质是什么?
(1)小明猜想另一种物质是Na2CO3,小军认为不可能.原因是:质量守恒定律.
为了证实小军的看法,请你设计一个证明CO32-不存在的实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 取样品,加入稀盐酸 | 没有气泡产生 | 生成物中没有CO32- |
[表 达]小军根据实验探究的结果,写出了过氧化钠和水反应的化学方程式为2Na2O2+2H2O═4NaOH+O2↑.
[发现问题]小娟发现在小军的实验中,试管中的溶液变成红色后,一会儿又变成无色.
[深入探究]实验三:探究滴入无色酚酞试液后,变成红色的溶液为什么会褪色?
小娟经查阅资料,设计了如下实验方案,并将有关现象记录在下表中.
| 实验序号 | 实验方案 | 实验现象 |
| 1 | 将水滴入盛有过氧化钠固体的试管中,配制成溶液,用带火星的木条检验生成的气体 | 反应激烈,有大量气体产生,并能使木条复燃 |
| 2 | 取三份实验1所得溶液分装于三支试管中是进行如下实验: ①第一份中加入紫色石蕊试液 ②第二份中加入无色酚酞试液 ③第三份中先加水再加入无色酚酞试液 | ①溶液变蓝且长时间不褪色 ②溶液显红色,半分钟内褪色 ③溶液显红色,半分钟内褪色 |
| 3 | ①称取3.9g过氧化钠固体,逐滴加入约50mL水. ②待不再产生气体,10min以后,加入用小纸片包好的MnO2,迅速塞紧双孔塞,轻轻摇动反应器,纸包自动散开,MnO2与溶液开始接触. | ①测得氧气体积为185mL左右 ②又产生大量氧气,至反应完全以后,又测得产生了374mL氧气(两次测定条件均相同) |
(2)综合分析上述实验,猜想使变红的酚酞褪色的物质是H2O2,请你用实验1所得的溶液,设计一个简单实验证明你的猜想在实验1所得溶液中加入少许MnO2,直到无气体产生时,再加入无色酚酞试液,溶液变红且不再褪色.
(3)根据实验3测得的气体体积说明了水与Na2O2反应生成的H2O2约有$\frac{1}{3}$发生分解.
分析 根据题干提供的信息进行分析,实验一:氧气能使带火星的木条复燃,过氧化钠与水的反应为放热反应,放出的热使温度升高,瓶内的压强增大,实验二:检验碳酸盐可以使用加酸化气的方法,酚酞试液在碱性溶液中变红,实验三:根据实验现象以及质量守恒定律可以推知还可能反应生成了过氧化氢,根据两次反应生成的氧气的体积即可推得反应的物质的量.
解答 解:实验一:(1)用带火星的木条靠近P处,木条复燃.说明生成的气体是氧气;
(2)过氧化钠与水的反应为放热反应,放出的热使温度升高,瓶内的压强增大,气体向外逸出,所以产生该现象的原因:过氧化钠与水反应放出热量,使瓶中的空气受热膨胀,因此伸入烧杯中的导管口看到有气泡产生;
实验二:(1)
小明猜想另一种物质是Na2CO3,小军认为不可能,原因是:质量守恒定律;’
检验碳酸盐可以使用加酸化气的方法,所以
| 实验步骤 | 实验现象 |
| 取少量反应后所得的溶液于试管中,加入稀盐酸 | 没有气泡产生 |
【表达】根据质量守恒定律反应除了生成氧气还生成了氢氧化钠,化学方程式为:2Na2O2+2H2O═4NaOH+O2↑;
实验三:(1)根据实验现象以及质量守恒定律可以推知还可能反应生成了过氧化氢,化学方程式为:Na2O2+2H2O═2NaOH+H2O2;
(2)氢氧化钠能使酚酞变红,水不能使酚酞褪色,可能是过氧化氢使酚酞褪色,H2O2,要证明是过氧化氢的原因,可以设计实验将过氧化氢反应掉,而又不生成显碱性的物质,观察酚酞是否变红即可,所以实验方案为:在实验1所得溶液中加入少许MnO2,直到无气体产生时,再加入无色酚酞试液,溶液变红且不再褪色;
(3)没加二氧化锰之前生成的氧气的体积为185mL,加入二氧化锰之后生成的氧气的体积为374mL,说明水与Na2O2反应生成的H2O2约有$\frac{1}{3}$发生分解;
【反思与评价】针对过氧化氢能使酚酞褪色,可以提出过氧化氢为什么能使酚酞褪色.
故答案为:(1)氧气;
(2)过氧化钠与水反应放出热量,使瓶中的空气受热膨胀,因此伸入烧杯中的导管口看到有气泡产生;
实验二:(1)
质量守恒定律
| 实验步骤 | 实验现象 |
| 取少量反应后所得的溶液于试管中,加入稀盐酸 | 没有气泡产生 |
【表达】2Na2O2+2H2O═4NaOH+O2↑;
实验三:(1)Na2O2+2H2O═2NaOH+H2O2;
(2)H2O2,在实验1所得溶液中加入少许MnO2,直到无气体产生时,再加入无色酚酞试液,溶液变红且不再褪色;
(3)水与Na2O2反应生成的H2O2约有$\frac{1}{3}$发生分解.
点评 本题为信息给予题,完成此类题目,要能够从题干中抽取有用的信息,根据已有的知识进行,同学们要能够从整体上把握题意,综合进行做题.

练习册系列答案
 期末集结号系列答案
期末集结号系列答案
相关题目
2.在如表的空格中写出相应的物质名称、化学式或物质的类别(指单质、氧化物、酸、碱、盐)
| 物质名称 | 氯气 | 氢氧化钙 | 碳酸钠 | ||
| 化学式 | Cl2 | Fe2O3 | Ca(OH)2 | H2SO4 | Na2CO3 |
| 物质类别 | 单质 | 氧化物 | 碱 | 酸 | 盐 |
19.硅(Si)是太阳能电池和电脑芯片不可缺少的材料.利用石英砂(主要成分为SiO2)生产高纯硅(Si)的流程图如下(整个制备过程必须达到无水、无氧气).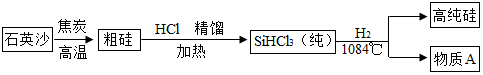
(提示:Si+3HCl$\frac{\underline{\;\;△\;\;}}{\;}$SiHCl3+H2↑)
根据以上信息判断,下列相关说法错误的是( )

(提示:Si+3HCl$\frac{\underline{\;\;△\;\;}}{\;}$SiHCl3+H2↑)
根据以上信息判断,下列相关说法错误的是( )
| A. | 三氯硅烷(SiHCl3)是由三种元素组成的物质 | |
| B. | 在H2和SiHCl3反应的过程中若混入O2,可能引起爆炸 | |
| C. | 以上生成高纯硅的流程中,可循环使用的物质只有HCl | |
| D. | Si+3HCl$\frac{\underline{\;\;△\;\;}}{\;}$SiHCl3+H2↑反应中硅元素的化合价未发生改变 |
6.把一定质量的a、b、c、d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质如下,下列说法中正确的是( )
| 物质 | a | b | c | d |
| 反应前的质量(g) | 6.4 | 3.2 | 2.8 | 4.0 |
| 反应后的质量(g) | 5.2 | X | 2.8 | 7.6 |
| A. | a和d是反应物 | B. | 该反应是化合反应 | ||
| C. | X=2.0g | D. | d一定是催化剂 |
7.如图所示的四个图象中,不能正确表示对应变化关系的是( )
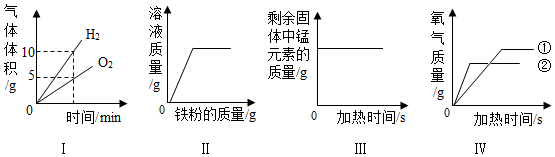
Ⅰ.电解水
Ⅱ.向一定量硫酸铜溶中不断加入铁粉
Ⅲ.加热一定量高锰酸钾固体
Ⅳ.用过氧化氢溶液分别在①有催化剂、②无催化剂的条件下制氧气.

Ⅰ.电解水
Ⅱ.向一定量硫酸铜溶中不断加入铁粉
Ⅲ.加热一定量高锰酸钾固体
Ⅳ.用过氧化氢溶液分别在①有催化剂、②无催化剂的条件下制氧气.
| A. | Ⅰ、Ⅱ | B. | Ⅰ、Ⅱ、Ⅲ | C. | Ⅱ、Ⅳ | D. | Ⅰ、Ⅱ、Ⅲ、Ⅳ |
14.焊接或切割金属常用氧炔焰.氧炔焰是乙炔(C2H2)气体和氧气反应产生的3000°C以上的高温火焰.乙炔由固体碳化钙(化学式为CaC2)与水反应制得,同时生成一种白色固体.
【提出问题】白色固体是什么物质?
【进行猜想】刘平同学认为有以下几种可能:
想一:CaO;猜想二:CaCO3;猜想三:Ca(OH)2.
的依据是根据质量守恒定律.
【交流评价】经过同学交流讨论,认为猜想一成立.否定猜想一的理由是:氧化钙与水反应也生成氢氧化钙.
【交流评价】
【实验结论】白色固体是Ca(OH)2.
出碳化钙与水反应制取乙炔的化学方程式:CaC2+2H2O=Ca(OH)2+C2H2↑.
【提出问题】白色固体是什么物质?
【进行猜想】刘平同学认为有以下几种可能:
想一:CaO;猜想二:CaCO3;猜想三:Ca(OH)2.
的依据是根据质量守恒定律.
【交流评价】经过同学交流讨论,认为猜想一成立.否定猜想一的理由是:氧化钙与水反应也生成氢氧化钙.
【交流评价】
| 实验操作 | 实验现象 | 结论 | |
| 实验一 | 取样于试管中,滴加稀盐酸 | 猜想二:不成立 | |
| 实验二 | 猜想三:成立 |
出碳化钙与水反应制取乙炔的化学方程式:CaC2+2H2O=Ca(OH)2+C2H2↑.
11.在一定条件下,下列的物质间的转化能一步实现是( )
①Fe→Fe3O4
②S→SO2
③CuSO4→Cu
④CaCO3→CaC12.
①Fe→Fe3O4
②S→SO2
③CuSO4→Cu
④CaCO3→CaC12.
| A. | ①②③ | B. | ①②④ | C. | ①③④ | D. | ①②③④ |