题目内容
实验室常用下列装置制取气体,请你根据所学知识回答下列问题.

(1)写出编号所指仪器的名称:① ;② .
(2)装置图中共有两处明显的错误,请你找出错误的地方并把改正的结果填在下列横线上:① ;② .
上述装置改进后,请继续回答下列问题.
(3)小李在实验室中用氯酸钾和另一种固体制取氧气,他选择上述装置中的A和 或 (填字母)进行组装.小红在实验室中选用C装置作为氧气的发生装置.在他们的实验中都用到了一种相同的固体药品是 (填化学式),请你写出小红制取氧气的化学反应方程式: .
(4)实验室选用C和E装置还可以制取的气体是 (填化学式),写出实验室制取该气体的化学方程式 .若用G装置收集该气体,该气体从 (填a或b)口进.
(5)装置B、C都可以用来制取(4)中的气体,比较这两个装置的不同,指出B装置的一个突出优点 .
(6)实验室常用加热氢氧化钙固体和氯化铵固体混合物的方法来制取氨气,已知氨气的密度小于空气,易溶于水且能和水反应.则实验室制取氨气的发生装置为 (填字母编号,下同),收集装置为 .

(1)写出编号所指仪器的名称:①
(2)装置图中共有两处明显的错误,请你找出错误的地方并把改正的结果填在下列横线上:①
上述装置改进后,请继续回答下列问题.
(3)小李在实验室中用氯酸钾和另一种固体制取氧气,他选择上述装置中的A和
(4)实验室选用C和E装置还可以制取的气体是
(5)装置B、C都可以用来制取(4)中的气体,比较这两个装置的不同,指出B装置的一个突出优点
(6)实验室常用加热氢氧化钙固体和氯化铵固体混合物的方法来制取氨气,已知氨气的密度小于空气,易溶于水且能和水反应.则实验室制取氨气的发生装置为
考点:常用气体的发生装置和收集装置与选取方法,实验室制取氧气的反应原理,二氧化碳的实验室制法,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)熟悉常见仪器,了解名称;
(2)图A中从防止冷凝液流回试管考虑;图E中导气管太短;
(3)过氧化氢分解可生产水、氧气;根据氧气的密度和溶水性选择收集装置;其中二氧化锰为催化剂;
(4)C和E装置还可以制取二氧化碳;据反应原理写出方程式;根据二氧化碳密度大于空气的密度分析;
(5)B装置可以控制反应的发生与结束;
(6)发生装置的选择要看反应物的状态和反应条件;收集装置的选择要看气体的密度和溶解性..
(2)图A中从防止冷凝液流回试管考虑;图E中导气管太短;
(3)过氧化氢分解可生产水、氧气;根据氧气的密度和溶水性选择收集装置;其中二氧化锰为催化剂;
(4)C和E装置还可以制取二氧化碳;据反应原理写出方程式;根据二氧化碳密度大于空气的密度分析;
(5)B装置可以控制反应的发生与结束;
(6)发生装置的选择要看反应物的状态和反应条件;收集装置的选择要看气体的密度和溶解性..
解答:解:(1)长颈漏斗方便加液体药品,集气瓶是收集气体的仪器,故答案为:长颈漏斗;集气瓶;
(2)A图中,为防止冷凝液倒流回试管,引起试管的炸裂,试管口应该略向下倾斜;E图中,用向上排空气法收集气体时,导气管伸入过短;故答案为:A中试管口向上倾斜了,试管口应该略向下倾斜;E中的导管太短了,导管应该伸到集气瓶的底部;
(3)因氧气的密度比空气大,不溶于水,收集装置选择E或F;制取装置包括加热和不需加热两种,如果用双氧水制氧气就不需要加热,如果用氯酸钾制氧气就需要加热,其中二氧化锰是固体,在两个反应中都气催化作用,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,配平即可2H2O2
2H2O+O2↑;
(4)实验室选用C和E装置还可以制取的气体是二氧化碳,反应的方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O;二氧化碳的密度大于空气的密度,若用G装置收集该气体,该气体从a口进入;
(5)比较两个装置可以发现B装置多一个开关和一个带小孔的隔板,假如关闭开关,随着气体的增多,内部压强随之增大,导致液体不能流入试管,使反应停止;
(6)根据反应装置和反应原理:固体+固体,且需要加热,及氨气的密度小于空气,易溶于水且能和水反应;所以用加热氢氧化钙固体和氯化铵固体混合物的方法来制取氨气的发生装置为A,收集装置为D;
故答案为:
(1)长颈漏斗;集气瓶;
(2)①A中试管口向上倾斜了,试管口应该略向下倾斜、②E中的导管太短了,导管应该伸到集气瓶的底部;
(3)E、F、MnO2、2H2O2
2H2O+O2↑;
(4)CO2、CaCO3+2HCl=CaCl2+CO2↑+H2O、a;
(5)可以使化学反应随开随停;
(6)A、D.
(2)A图中,为防止冷凝液倒流回试管,引起试管的炸裂,试管口应该略向下倾斜;E图中,用向上排空气法收集气体时,导气管伸入过短;故答案为:A中试管口向上倾斜了,试管口应该略向下倾斜;E中的导管太短了,导管应该伸到集气瓶的底部;
(3)因氧气的密度比空气大,不溶于水,收集装置选择E或F;制取装置包括加热和不需加热两种,如果用双氧水制氧气就不需要加热,如果用氯酸钾制氧气就需要加热,其中二氧化锰是固体,在两个反应中都气催化作用,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,配平即可2H2O2
| ||
(4)实验室选用C和E装置还可以制取的气体是二氧化碳,反应的方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O;二氧化碳的密度大于空气的密度,若用G装置收集该气体,该气体从a口进入;
(5)比较两个装置可以发现B装置多一个开关和一个带小孔的隔板,假如关闭开关,随着气体的增多,内部压强随之增大,导致液体不能流入试管,使反应停止;
(6)根据反应装置和反应原理:固体+固体,且需要加热,及氨气的密度小于空气,易溶于水且能和水反应;所以用加热氢氧化钙固体和氯化铵固体混合物的方法来制取氨气的发生装置为A,收集装置为D;
故答案为:
(1)长颈漏斗;集气瓶;
(2)①A中试管口向上倾斜了,试管口应该略向下倾斜、②E中的导管太短了,导管应该伸到集气瓶的底部;
(3)E、F、MnO2、2H2O2
| ||
(4)CO2、CaCO3+2HCl=CaCl2+CO2↑+H2O、a;
(5)可以使化学反应随开随停;
(6)A、D.
点评:学会比较用碳酸钙与盐酸制取二氧化碳、用氯酸钾制取氧气和用过氧化氢溶液和二氧化锰制取氧气的区别联系;掌握制取氧气和二氧化碳的反应原理、制法及操作步骤和注意点;了解催化剂的特点与催化作用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列叙述中正确的是( )
| A、二氧化碳气体通入氢氧化钠溶液时,溶液增加的质量就是被吸收的二氧化碳的质量 |
| B、按任意体积混合后的氢气和氧气的总质量,跟反应后生成水的质量相等 |
| C、镁带在空气中燃烧后,生成物的质量跟原镁带的质量相等 |
| D、煤球燃烧后质量减轻,这不符合质量守恒定律 |
今有四种粒子的结构示意图,下列说法正确的是( )
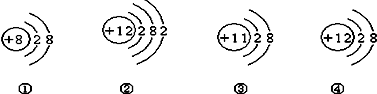

| A、它们表示四种元素 |
| B、④表示的元素是非金属元素 |
| C、②④是同种元素 |
| D、①④表示的是阳离子 |