题目内容
下列叙述中正确的是( )
| A、二氧化碳气体通入氢氧化钠溶液时,溶液增加的质量就是被吸收的二氧化碳的质量 |
| B、按任意体积混合后的氢气和氧气的总质量,跟反应后生成水的质量相等 |
| C、镁带在空气中燃烧后,生成物的质量跟原镁带的质量相等 |
| D、煤球燃烧后质量减轻,这不符合质量守恒定律 |
考点:质量守恒定律及其应用,二氧化碳的化学性质
专题:化学用语和质量守恒定律
分析:由题意可知,所列四种现象都是化学反应,那么是化学反应就必定遵循质量守恒定律,参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和.根据质量守恒定律不难判断A、B、C、D四个选项所述的正误.
解答:解:A、二氧化碳为酸性气体,溶于水形成碳酸,再与氢氧化钠发生酸碱中和反应产生盐,因而会使溶液质量增加.据质量守恒定律可知,溶液增加的质量就是被吸收的二氧化碳的质量.所以A选项正确;
B、氢气和氧气点燃充分反应后生成水,化学方程式如下:2H2+O2
2H2O,由化学方程式可见,当氢气跟氧气的体积比为2:1时,才能恰好完全反应.否则,必有一种会剩余,那生成水的质量就不是两种气体质量的和.所以B选项不正确;
C、根据质量守恒定律,镁带在空气中燃烧后生成氧化镁,质量会增加,所以C选项叙述不正确;
D、煤的主要成分是碳,燃烧后会生成二氧化碳,如果不是在密闭的装置中二氧化碳会泄露.煤球燃烧后质量减轻主要是因为二氧化碳气体的逃逸,煤球燃烧既然是化学反应那它一定遵循质量守恒定律.因此D选项叙述错误.
故选A.
B、氢气和氧气点燃充分反应后生成水,化学方程式如下:2H2+O2
| ||
C、根据质量守恒定律,镁带在空气中燃烧后生成氧化镁,质量会增加,所以C选项叙述不正确;
D、煤的主要成分是碳,燃烧后会生成二氧化碳,如果不是在密闭的装置中二氧化碳会泄露.煤球燃烧后质量减轻主要是因为二氧化碳气体的逃逸,煤球燃烧既然是化学反应那它一定遵循质量守恒定律.因此D选项叙述错误.
故选A.
点评:本题以选择题的形式考查了质量守恒定律,只要是化学反应必定遵循质量守恒定律,注意分析参加反应和生成的所有物质,否则会使质量增加或减小.

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
除去N2中混有的O2,下列方法中可行的是( )
| A、将混合气体通过灼热的炭层 |
| B、将混合气体通过灼热的铜网 |
| C、用倾倒法分离 |
| D、将混合气体通过灼热的硫粉 |
在托盘天平两边各放一只等质量的烧杯,在两只烧杯里分别加入50g溶质质量分数为7.3%的稀盐酸,将天平调节至平衡;然后向左右两烧杯中分别加入一定质量的下列各组物质,充分反应后,天平发生偏转的是( )
| A、1.8g铝粉和1.8g 铁粉 |
| B、4.2g碳酸镁和2g硝酸银 |
| C、5.6g铁粉和5.6g 锌粉 |
| D、10g碳酸钙和5.6g氧化钙 |
KMnO4和K2MnO4两种物质中都含有Mn元素,其中Mn元素的化合价分别为( )
| A、+5和+7 |
| B、+7和+5 |
| C、+6和+7 |
| D、+7和+6 |
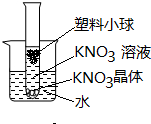 如图所示,烧杯中盛有一定量的水,试管中盛有一定量的有少量固体存在的硝酸钾溶液,在溶液中悬浮着一只塑料小球,请回答下面问题.
如图所示,烧杯中盛有一定量的水,试管中盛有一定量的有少量固体存在的硝酸钾溶液,在溶液中悬浮着一只塑料小球,请回答下面问题.