题目内容
6.在一个密闭容器内有X、Y、Z、R在一定条件下反应一段时间后,测得反应前后各物质的质量如下:| 物质 | X | Y | Z | R |
| 反应前质量(g) | 10 | 10 | 10 | 10 |
| 反应后质量(g) | 0 | 10 | 12 | 18 |
(1)反应物为X,生成物为Z、R,催化剂为Y.
(2)此反应的反应基本类型为分解反应.
分析 在化学反应中,如果反应前后物质的质量没有发生变化,这种可能是催化剂或没有参加反应,如果反应后质量增加了,该物质是生成物,如果反应后质量减小了,那么该物质是反应物.
解答 解:由表可以发现反应后X的质量减少,是反应物,ZR质量增大,是生成物,Y反应前后物质的质量没有发生变化,可能是催化剂.本反应是一种物质反应生成了二种新物质的反应,属于分解反应.
故填:(1)X; Z、R;Y (2)分解反应.
点评 解答这类题关键是要会运用质量守恒定律的含义:参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
16.下列叙述中错误的是( )
| A. | 食盐仅仅是一种调味品 | |
| B. | 食盐是一种重要的化工原料 | |
| C. | 利用食盐可以制造漂白粉、肥皂和农药等 | |
| D. | 食盐也可以间接用于造纸、纺织和印染等工业 |
17.不同的球体代表不同的原子,下列说法中,不正确的是( )
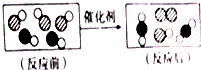

| A. | 分子在化学变化中可分 | |
| B. | 化学反应前后,原子种类不变 | |
| C. | 参加反应的两种分子的个数比为3:2 | |
| D. | 生成物中有单质 |
14.下列物质中,属于纯净物的是( )
| A. | 冰水混合物 | B. | 清澈的井水 | C. | 洁净的空气 | D. | 雪碧饮料 |
11.石灰石是生产玻璃、氯化钙等多种化工产品的原料.某研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数,取来了矿石样品,并取稀盐酸200g,平均分成4份,进行实验,结果如下:
(1)第3、4次反应中矿石有剩余;
(2)表中m值是4.4;
(3)试计算这种石灰石中碳酸钙的质量分数.
| 实 验 | 1 | 2 | 3 | 4 |
| 加入样品质量/g | 5 | 10 | 15 | 20 |
| 生成CO2的质量/g | 1.76 | 3.52 | 4.4 | m |
(2)表中m值是4.4;
(3)试计算这种石灰石中碳酸钙的质量分数.
18.下列物质与滴有酚酞试剂的石灰水恰好完全反应后,溶液还是呈红色的是( )
| A. | 碳酸钠 | B. | 盐酸 | C. | 二氧化碳 | D. | 硫酸铜 |
15.在托盘天平两边各放一只烧杯,调节至平衡.在两只烧杯里注入相同质量、相同质量分数的稀盐酸,然后分别放入质量相等的镁和铝.待充分反应后,镁有剩余,则还可以观察到的现象是( )
①天平保持平衡 ②铝也有剩余 ③天平指针偏向放镁的一方
④天平指针偏向放铝的一方 ⑤铝完全溶解.
①天平保持平衡 ②铝也有剩余 ③天平指针偏向放镁的一方
④天平指针偏向放铝的一方 ⑤铝完全溶解.
| A. | ②③ | B. | ①② | C. | ①⑤ | D. | ④⑤ |
16.现有镁和铁的混合物4克与足量的稀硫酸反应产生了氢气0.2克,则混合物中铁的质量分数是多少( )
| A. | 30% | B. | 70% | C. | 56% | D. | 24% |