题目内容
10.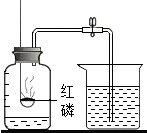 如图所示为某化学兴趣小组的一次实验装置及药品.
如图所示为某化学兴趣小组的一次实验装置及药品.(1)此实验的目的是测定空气中氧气的体积分数.
(2)为获得较为准确的实验数据,下列做法正确的是ABC.
A.确保装置的气密性良好
B.燃烧匙中的红磷足量
C.红磷熄灭,广口瓶冷却至室温后打开弹簧夹
D.点燃红磷后缓慢将燃烧匙插入瓶中,塞紧瓶塞
(3)红磷燃烧反应的文字表达式是磷+氧气$\stackrel{点燃}{→}$五氧化二磷,实验后小组同学讨论可否用木炭代替红磷,老师告诉他选用木炭不行,不能用木炭的原因是木炭燃烧会有二氧化碳产生.
分析 根据测定空气中氧气含量的原理分析,测定空气中氧气的物质应该具备的条件是:能和空气中的氧气反应,生成物是固体,不能和空气中的其它物质发生化学反应.
解答 解:(1)由实验的装置可知,此实验的目的是测定空气中氧气的体积分数.
(2)由测定空气中氧气含量的原理可知:
A.确保装置的气密性良好,故A正确;
B.燃烧匙中的红磷足量,将集气瓶中的氧气全部消耗掉,故B正确;
C.红磷熄灭,广口瓶冷却至室温后打开弹簧夹,故D正确;
D.点燃红磷后缓慢将燃烧匙插入瓶中,塞紧瓶塞
(3)红磷燃烧生成了五氧化二磷,反应的文字表达式是:磷+氧气$\stackrel{点燃}{→}$五氧化二磷,实验后小组同学讨论可否用木炭代替红磷,老师告诉他选用木炭不行,不能用木炭的原因是木炭燃烧会有二氧化碳产生.
故答为:(1)测定空气中氧气的体积分数;(2)ABC;(3)磷+氧气$\stackrel{点燃}{→}$五氧化二磷,木炭燃烧会有二氧化碳产生
点评 本题的难度不大,了解测定空气中氧气的含量实验的原理是解答本题的基础.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.下列实验操作中,正确的是( )
| A. |  给试管内液体加热 | B. |  向试管中滴加液体 | ||
| C. |  过滤液体 | D. |  向试管中倾倒液体 |
18.儿童缺钙易导致佝偻病,葡萄糖酸钙口服液是一种常用的补钙剂,这里描述的“钙”是指( )
| A. | 离子 | B. | 原子 | C. | 元素 | D. | 分子 |
15.下列关于物质在氧气中燃烧的实验现象描述正确的是( )
| A. | 镁在氧气中燃烧时,发出耀眼的白光,生成氧化镁 | |
| B. | 将空气中燃着的硫伸入氧气瓶中,火焰由黄色变为蓝紫色 | |
| C. | 磷在氧气中燃烧时,产生大量白烟 | |
| D. | 铁丝在空气中燃烧时,火星四射,有黑色固体生成 |
2.化学兴趣小组的同学准备探究实验所用石灰石中碳酸钙的质量.
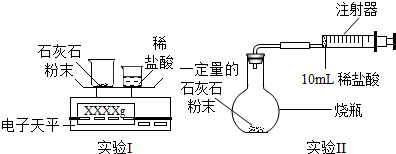
【提出方案】利用石灰石(主要成分为碳酸钙)与稀盐酸反应来测定生成CO2的质量和体积,并处理数据.
【资料】
1.实验Ⅰ、Ⅱ中石灰石样品(杂质不考虑)质量相等
2.通常情况下,二氧化碳的密度约为2.0克/升
3.化学反应前后元素的种类和质量均不变
【实验设计】通过下列两个实验分别测定CO2的质量和体积:
【分析与表达】
(1)实验I中,将小烧杯中的所有稀盐酸分几次全部加入到大烧杯中,并不断搅拌,判断石灰石中碳酸钙完全反应的操作及实验现象是:最后一次加入稀盐酸,仍没有气泡产生.
(2)实验II中,先连接好装置,再检查装置的气密性(填操作名称),然后装好药品,最后将10ml稀盐酸快速推入烧瓶中,若稀盐酸是缓慢推入的,则可能造成的后果是稀盐酸难以完全推入烧瓶中或仪器连接处脱落.
【记录与处理】
(3)已知实验I反应前的总质量【m(大烧杯+石灰石粉末)+m(小烧杯+稀盐酸)】,要计算生成CO2的质量,至少还需要的数据是AC.(填字母)
A.m(小烧杯) B.m(大烧杯) C.m(大烧杯+反应后剩余物)
(4)根据(3)计算得二氧化碳的质量为0.176克,实验中不可以(填“可以”或“不可以”)使用托盘天平.忽略其他因素影响,试计算石灰石样品中碳酸钙的质量.写出计算过程:0.4g.
(5)实验II的实验记录如下(表中数据在相同温度、相同压强条件下测定):
根据以上实验过程和数据综合分析,最终生成CO2的体积是88.0ml,理由是原稀盐酸占有10mL体积.
【反思与评价】
(6)请你综合各方面原因分析,你认为实验Ⅰ的优点是实验操作简单或便于读数,实验Ⅱ的优点是在密闭体系内反应更加环保.

【提出方案】利用石灰石(主要成分为碳酸钙)与稀盐酸反应来测定生成CO2的质量和体积,并处理数据.
【资料】
1.实验Ⅰ、Ⅱ中石灰石样品(杂质不考虑)质量相等
2.通常情况下,二氧化碳的密度约为2.0克/升
3.化学反应前后元素的种类和质量均不变
【实验设计】通过下列两个实验分别测定CO2的质量和体积:
【分析与表达】
(1)实验I中,将小烧杯中的所有稀盐酸分几次全部加入到大烧杯中,并不断搅拌,判断石灰石中碳酸钙完全反应的操作及实验现象是:最后一次加入稀盐酸,仍没有气泡产生.
(2)实验II中,先连接好装置,再检查装置的气密性(填操作名称),然后装好药品,最后将10ml稀盐酸快速推入烧瓶中,若稀盐酸是缓慢推入的,则可能造成的后果是稀盐酸难以完全推入烧瓶中或仪器连接处脱落.
【记录与处理】
(3)已知实验I反应前的总质量【m(大烧杯+石灰石粉末)+m(小烧杯+稀盐酸)】,要计算生成CO2的质量,至少还需要的数据是AC.(填字母)
A.m(小烧杯) B.m(大烧杯) C.m(大烧杯+反应后剩余物)
(4)根据(3)计算得二氧化碳的质量为0.176克,实验中不可以(填“可以”或“不可以”)使用托盘天平.忽略其他因素影响,试计算石灰石样品中碳酸钙的质量.写出计算过程:0.4g.
(5)实验II的实验记录如下(表中数据在相同温度、相同压强条件下测定):
| 时间/min | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 注射器读数/ml | 60.0 | 85.0 | 92.0 | 95.0 | 97.5 | 97.8 | 97.9 | 98.0 | 98.0 | 98.0 |
【反思与评价】
(6)请你综合各方面原因分析,你认为实验Ⅰ的优点是实验操作简单或便于读数,实验Ⅱ的优点是在密闭体系内反应更加环保.
19.通过下列图示实验得出的结论中正确的是( )

| A. | 图1可以粗略测定空气里氧气的含量 | |
| B. | 图2探究微粒在不停地运动 | |
| C. | 图3所示实验既说明电解水生成氢气和氧气,又说明水是由氢气和氧气组成的 | |
| D. | 图3制得的氢气和氧气的质量比为2:1 |

 如图所示.无色液体A和黑色粉末B混合后,生成尤色液体C和能使带火星的木条复燃的气体D,将烧得红热的金属E伸入集满气体D的集气瓶中生成F.
如图所示.无色液体A和黑色粉末B混合后,生成尤色液体C和能使带火星的木条复燃的气体D,将烧得红热的金属E伸入集满气体D的集气瓶中生成F.