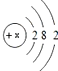
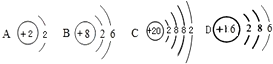题目内容
2.化学兴趣小组的同学准备探究实验所用石灰石中碳酸钙的质量.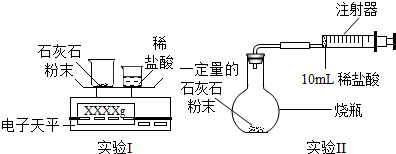
【提出方案】利用石灰石(主要成分为碳酸钙)与稀盐酸反应来测定生成CO2的质量和体积,并处理数据.
【资料】
1.实验Ⅰ、Ⅱ中石灰石样品(杂质不考虑)质量相等
2.通常情况下,二氧化碳的密度约为2.0克/升
3.化学反应前后元素的种类和质量均不变
【实验设计】通过下列两个实验分别测定CO2的质量和体积:
【分析与表达】
(1)实验I中,将小烧杯中的所有稀盐酸分几次全部加入到大烧杯中,并不断搅拌,判断石灰石中碳酸钙完全反应的操作及实验现象是:最后一次加入稀盐酸,仍没有气泡产生.
(2)实验II中,先连接好装置,再检查装置的气密性(填操作名称),然后装好药品,最后将10ml稀盐酸快速推入烧瓶中,若稀盐酸是缓慢推入的,则可能造成的后果是稀盐酸难以完全推入烧瓶中或仪器连接处脱落.
【记录与处理】
(3)已知实验I反应前的总质量【m(大烧杯+石灰石粉末)+m(小烧杯+稀盐酸)】,要计算生成CO2的质量,至少还需要的数据是AC.(填字母)
A.m(小烧杯) B.m(大烧杯) C.m(大烧杯+反应后剩余物)
(4)根据(3)计算得二氧化碳的质量为0.176克,实验中不可以(填“可以”或“不可以”)使用托盘天平.忽略其他因素影响,试计算石灰石样品中碳酸钙的质量.写出计算过程:0.4g.
(5)实验II的实验记录如下(表中数据在相同温度、相同压强条件下测定):
| 时间/min | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 注射器读数/ml | 60.0 | 85.0 | 92.0 | 95.0 | 97.5 | 97.8 | 97.9 | 98.0 | 98.0 | 98.0 |
【反思与评价】
(6)请你综合各方面原因分析,你认为实验Ⅰ的优点是实验操作简单或便于读数,实验Ⅱ的优点是在密闭体系内反应更加环保.
分析 (1)根据石灰石和盐酸反应放出二氧化碳气体进行解答;
(2)根据制取气体要先检查装置的气密性进行解答;
(3)根据反应前后物质质量差就是生成二氧化碳的质量进行解答;
(4)根据托盘天平的精确程度以及化学方程式进行分析计算;
(5)根据从第8分钟后气体的体积不再变化来分析;
(6)根据实验I的优点是操作简单,而实验II的优点现象更加直观进行解答.
解答 解:(1)石灰石和盐酸反应放出二氧化碳气体,所以,判断石灰石中CaCO3完全反应的实验现象是最后一次加入稀盐酸,仍没有气泡产生;
故填:仍没有气泡产生;
(2)制取气体要先检查装置的气密性;然后装好药品,最后将10ml稀盐酸快速推入烧瓶中.若稀盐酸是缓慢推入的,则可能造成的后果是烧瓶内气压增大,稀盐酸难以完全推入烧瓶中或仪器连接处脱落;
故填:检查装置的气密性;稀盐酸难以完全推入烧瓶中或仪器连接处脱落;
(3)根据反应前后物质质量差就是生成二氧化碳的质量,已知实验I反应前的总质量[m(大烧杯+石灰石粉末)+m(小烧杯+稀盐酸)],所以要计算生成CO2的质量,至少还需要的数据是m(小烧杯)和m(大烧杯+反应后剩余物);
故填:AC;
(4)托盘天平只能精确到0.1g,故不能使用托盘天平来称量;设其中碳酸钙的质量为x,则
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 0.176g
$\frac{100}{44}=\frac{x}{0.176g}$
x=0.4g
故填:不可以;0.4g;
(5)从第8分钟后气体的体积不再变化,但原稀盐酸占有10mL(推入稀盐酸后仍然会恢复到原压强),所以第1分钟生成CO2的体积是50.0mL,第2分钟是75.5mL,最终生成CO2的体积是88.0mL;故填:88.0;原稀盐酸占有10mL体积;
(6)实验I的优点是操作简单,而实验II的优点现象更加直观、环保.
故填:实验操作简单或便于读数;在密闭体系内反应更加环保.
点评 掌握装置气密性检验一般方法,本题主要考查分析和应用信息解答实际问题的能力,要结合物质的性质和反应规律进行综合分析.

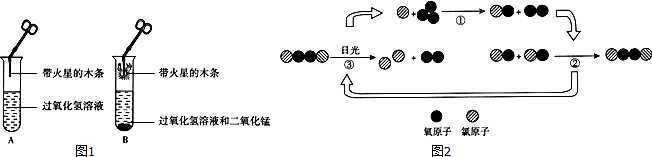
【实验1】验证二氧化锰是过氧化氢分解反应的催化剂
某同学设计如下实验:分别取5mL5%的过氧化氢溶液于两支试管中,向B中试管内加入少量二氧化锰(如图1所示).A中带火星的木条不复燃,B中带火星的木条复燃.
A中木条不复燃的原因是氧气的浓度不够或没有氧气产生,B中反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
有同学认为上述实验方案不足以证明二氧化锰是该反应的催化剂,理由是不能证明二氧化锰在反应前后的质量和化学性质没有改变.
【实验2】为探究二氧化锰对氯酸钾分解的催化作用.在相同条件下,同学们按下表进行实验,并记录相关数据.(其他影响实验的因素均相同)
| 编号 | KC103 质量/g | 其他物质质量/g | 待测数据 |
| 实验1 | 2.0 | / | |
| 实验2 | a | Mn02 0.5 |
②表中的待测数据指D(填字母序号).
A.氧气的质量 B.反应后固体的质量
C.氧气的体积 D.单位时间内产生氧气的体积
③设计“实验1”的目的是对比.
【拓展】
(1)同学们继续探究二氧化锰是否参与了氯酸钾的分解反应.
氯酸钾和二氧化锰混合加热的化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KC1+302↑.已知氯酸钾与二氧化锰混合加热时连续发生如下反应,试分析后按要求填空.
(I)2KC103+2Mn02$\frac{\underline{\;\;△\;\;}}{\;}$2KMn04+Cl2↑+02↑;
(Ⅱ)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑(用化学方程式表示);
(Ⅲ)K2Mn04+Cl2$\frac{\underline{\;\;△\;\;}}{\;}$2KCl+Mn02+02↑.
通过以上分析,同学们得出结论:二氧化锰参与了氯酸钾的分解反应.
(2)氟利昂释放出的氯原子参与了臭氧层的破坏,其他微观示意图如图2,综合图中①②③的反应过程,写出臭氧层被破坏的化学方程式:2O3$\frac{\underline{\;\;\;CL\;\;\;}}{日光}$3O2.
| A. | 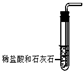 制取CO2 | B. | 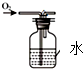 监控气体流速 | C. | 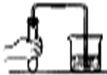 检查装置气密性 | D. |  验证O2的性质 |
| A. | 钻石(C) | B. | 食盐(NaCl) | C. | 水晶(SiO2) | D. | 氯酸钾(KClO3) |
 将分别蘸有浓氨水和浓盐酸的两根玻璃棒靠近(不接触)如图,可观察到大量白烟.根据这一实验现象得出的以下结论错误的是( )
将分别蘸有浓氨水和浓盐酸的两根玻璃棒靠近(不接触)如图,可观察到大量白烟.根据这一实验现象得出的以下结论错误的是( )| A. | 这一过程仅发生物理变化 | B. | 分子在不停地运动 | ||
| C. | 浓盐酸,浓氨水具有挥发性 | D. | 化学反应前后,分子种类发生改变 |
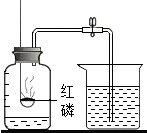 如图所示为某化学兴趣小组的一次实验装置及药品.
如图所示为某化学兴趣小组的一次实验装置及药品.